
【题目】现有含少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示
注:KNO3固体容易受热分解;HNO3易挥发.
(1)沉淀A的主要成分是、(填化学式).
(2)②中反应的化学方程式是 .
(3)③进行的实验操作是(填操作名称).
(4)③加入过量的K2CO3溶液的目的是 .
(5)为了除去溶液3中的杂质,可向其中加入适量的 . 从此溶液获得KNO3晶体的操作是、、过滤.
【答案】
(1)BaSO4;BaCO3
(2)AgNO3+KCl═AgCl↓+KNO3
(3)过滤
(4)Ba2+、Ag+
(5)稀硝酸;蒸发浓缩;冷却结晶
【解析】解:利用含少量KCl、K2SO4、K2CO3杂质的KNO3溶液,得到纯净的KNO3固体,由流程可知,①中加过量的硝酸钡,与K2SO4、K2CO3反应生成沉淀A为BaSO4、BaCO3 , 滤液中含KCl、硝酸钡、KNO3 , ②中与过量硝酸银反应生成AgCl沉淀,溶液2中含硝酸钡、硝酸银、硝酸钾,③中与过量碳酸钾反应生成碳酸钡、碳酸银沉淀,溶液3中含硝酸钾、碳酸钾,应加硝酸再蒸发结晶、过滤得到硝酸钾,(1)由上述分析可知,沉淀A中含BaSO4、BaCO3 , 所以答案是:BaSO4;BaCO3;(2)②中反应的化学方程式AgNO3+KCl═AgCl↓+KNO3 , 所以答案是:AgNO3+KCl═AgCl↓+KNO3;(3)③分离不溶性固体与溶液,进行的实验操作是过滤,所以答案是:过滤;(4)③加入过量的K2CO3溶液的目的是除去Ba2+、Ag+ , 所以答案是:Ba2+、Ag+;(5)为了除去溶液3中的杂质,可向其中加入适量的稀硝酸.从此溶液获得KNO3晶体的操作是蒸发浓缩、冷却结晶、过滤,所以答案是:稀硝酸;蒸发浓缩;冷却结晶.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】对某酸性溶液(可能含有Br﹣ , SO42﹣ , H2SO3 , NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸.
对于下列物质不能确认其在原溶液中是否存在的是( )
A.Br﹣
B.SO42﹣
C.H2SO3
D.NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下微粒含配位键的是( )
①N2H5+ ②CH4 ③OH﹣ ④NH4+ ⑤Fe(CO)5⑥Fe(SCN)3⑦H3O+
⑧[Ag(NH3)2]OH ⑨[B(OH)4]﹣ .
A.①②④⑦⑧
B.③④⑤⑥⑦⑨
C.①④⑤⑥⑦⑧⑨
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda﹣style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( ) 
A.分子式为C20H20
B.一氯代物的同分异构体只有两种
C.分子中含有二个亚甲基(﹣CH2﹣)
D.分子中含有4个五元碳环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(化学式为H2C2O4 , 是一种二元酸)存在于自然界的植物中.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是有气泡冒出且澄清石灰水变浑浊,由此可知草酸晶体分解的产物中有 . 装置B的主要作用是冷凝(水蒸气和草酸),防止草酸进入装置C中发生反应(填化学方程式),干扰分解生成气体的检验.
(2)乙组同学认为草酸晶体分解的产物中还可能含有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置进行实验.
①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G、H、D、I.其中装置F中发生的化学反应为 . 两次使用了D装置,其中第一个D装置的作用是 , 装置H反应管中盛有的物质是 .
②能证明草酸晶体分解产物中有CO的现象是H中物质变为色;且 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干电池原理如图所示,电池总反应为Zn+2NH4+═Zn2++2NH3↑+H2↑.下列说法正确的是( ) 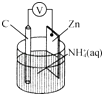
A.碳电极上发生还原反应
B.Zn极上发生还原反应
C.常见锌锰干电池为二次电池
D.负极上发生的反应为2NH4++2e﹣═2NH3↑+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K= ![]() .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2OCO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com