
【题目】铁红(Fe2O3)是一种常见颜料,用废铁屑制取铁红的工艺如图:

(1)写出废铁屑中的铁和稀硫酸反应的离子方程式:_____。
(2)“沉淀”反应中除生成FeCO3外,还生成一种能使澄清石灰水变浑浊的气体,该气体为_____。
(3)检验滤液中含有![]() 的方法是_____。
的方法是_____。
(4)“煅烧”时FeCO3与O2反应的物质的量之比为_____。
【答案】Fe+2H+=H2↑+Fe2+ CO2 取少许滤液于试管中,向其中加入NaOH浓溶液,加热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝,则滤液中含有![]() 4∶1
4∶1
【解析】
(1)铁和稀硫酸反应的离子方程式:Fe+2H+=H2↑+Fe2+;
(2)“沉淀”反应中加入碳酸氢铵,除生成FeCO3外,还生成一种能使澄清石灰水变浑浊的气体,则该气体一定为二氧化碳;
(3)![]() 在碱性条件下生成氨气,显碱性,故检验滤液中含有
在碱性条件下生成氨气,显碱性,故检验滤液中含有![]() :取少许滤液于试管中,向其中加入NaOH浓溶液,加热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝,则滤液中含有
:取少许滤液于试管中,向其中加入NaOH浓溶液,加热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝,则滤液中含有![]() ;
;
(4)根据氧化还原反应配平原理可知,“煅烧”时FeCO3与O2反应生成铁红(氧化铁):![]() ,故FeCO3与O2反应的物质的量之比为4∶1。
,故FeCO3与O2反应的物质的量之比为4∶1。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】6.4g铜投入一定浓度的HNO3中,铜完全溶解,生成NO和NO2的混合气体,用试管全部收集,得到标准状况下的体积为2240mL。请回答:
(1)反应中消耗掉HNO3的物质的量为___mol。
(2)生成NO2的体积(标况)为___mL。
(3)将盛有混合气体的试管倒扣在水槽中,通入标况下的O2,恰好使气体完全溶于水中,则通入O2的体积是___mL。(请写出解答过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:____________。
(2)实验室中用过氧化氢制取氧气的化学方程式为_______________,当生成标准状况下2.24L O2时,转移电子为______ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在其水溶液中的电离方程式:______。(只写第一步)
(4)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确:___________
Ⅱ.工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
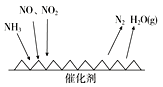
(1)由上图可知SCR技术中的氧化剂为________。
(2)用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________________________________
Ⅲ.研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应①:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
CH3OH(g)+H2O(g) △H1= -49.6 kJ/mol
反应②:CH3OCH3(g)+H2O(g)![]() 2CH3OH(g) △H2= +23.4 kJ/mol
2CH3OH(g) △H2= +23.4 kJ/mol
反应③:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=___________kJ/mol。
CH3OCH3(g)+3H2O(g) △H3=___________kJ/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中的信息判断,下列说法错误的是

A. 第①组反应的氧化产物为O2
B. 第②组反应中C12与FeBr2的物质的量之比小于或等于1:2
C. 第③组反应中生成3mol C12,转移6mol电子
D. 氧化性由强到弱的顺序为C1O3- >C12>Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列方法均可制得氯气:①MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A.15∶5∶3B.1∶3∶5C.6∶5∶6D.1∶6∶10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是_______,一定互为同分异构体的是________________(填编号);
(2)以五倍子为原料可制得A,A结构简式为下图所示,回答下列问题:
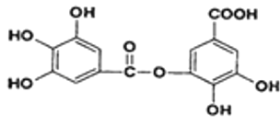
①A的分子式为______________;
②有机化合物B在硫酸催化条件下加热发生酯化可得到A。写出B的结构简式为_____ ;
(3)写出含有1个-CH2-、1个![]() 、3个-CH3原子团的烃类物质的结构简式___________;
、3个-CH3原子团的烃类物质的结构简式___________;
(4)写出核磁共振氢谱有两组峰,且峰面积之比为3:2,分子式为C8H10的芳香烃类化合物的结构简式_________;
(5)写出该有机物的名称![]() ________________。
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 均为短周期元素,它们在元素周期表中的位置如图所示, ,若 W 原子的最外层电子数是内层电子总数的
,若 W 原子的最外层电子数是内层电子总数的![]() ,下列说法中正确的是( )
,下列说法中正确的是( )
A.阴离子的半径从大到小排列顺序为X>Y>Z>W
B.X、Y、Z、W元素的氢化物分子间都可以形成氢键
C.Y的两种同素异形体在常温下可以相互转化
D.最高价氧化物对应的水化物的酸性:W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如下:回答下列问题:
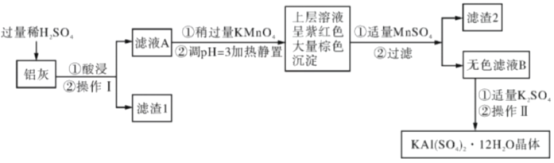
(1)明矾净水的原理是____________(用离子方程式表示)。
(2)操作Ⅱ是蒸发浓缩、__________、过滤、__________、干燥,
(3)检验滤液A中是否存在Fe2+的试剂是________________(只用一种试剂)。
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是_________,在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO4-转化为Mn2+):________
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:_________________,滤渣2含有的物质是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,可逆反应mA(g)+nB(g)![]() pC(g)的平衡常数为K,下列对K的说法正确的是( )
pC(g)的平衡常数为K,下列对K的说法正确的是( )
A.K值越大,表明该反应越有利于C的生成
B.若缩小反应器的容积,能使平衡正向移动,则K增大
C.温度越高,K一定越大
D.如果m+n=p,则K=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com