
目前,新能源不断被应用到现代的汽车中,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是________。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4
3NaClO+2Fe(NO3)3+10NaOH===2Na2FeO4↓+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4
Na2FeO4+2KOH===K2FeO4↓+2NaOH
主要的生产流程如下:

①写出反应①的离子方程式________________________________________________。
②流程图中“转化”(反应③)是在某低温下进行的,且此温度无NaOH析出,说明此温度下Ksp(K2FeO4)____Ksp(Na2FeO4)(填“>”、“<”或“=”)。
(3)已知K2FeO4在水溶液中可以发生:__FeO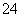 +__H2O__Fe(OH)3↓+__OH-+__O2↑,配平上述方程式K2FeO4在水处理中的作用是__________________。
+__H2O__Fe(OH)3↓+__OH-+__O2↑,配平上述方程式K2FeO4在水处理中的作用是__________________。
(4)FeO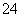 在水溶液中的存在形态如图所示:
在水溶液中的存在形态如图所示:
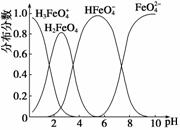
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO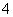 的分布分数的变化情况是________。
的分布分数的变化情况是________。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,________转化为____________(填化学式)。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
烧碱、纯碱等都是重要的化工原料。
(1)利用如图装置可以证明二氧化碳与烧碱溶液发生了反应。
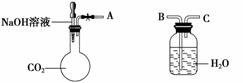
①若将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是________________________________________________________________________。
②若其他操作不变,将A与C连接,可观察到的现象是________________________。
(2)向100 mL 1 mol·L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,按出现的先后顺序分别是Ⅰ.NaOH、Na2CO3,Ⅱ.__________________,Ⅲ.Na2CO3、NaHCO3,Ⅳ.__________________。
①常温下,将得到的固体X重新溶于水,在所得溶液中加入盐酸,使溶液的pH=7,再将溶液蒸干,得到固体的质量为________ g。
②若要验证白色固体X是第Ⅰ种组成,依次加入的试剂为________(填字母序号)。
a.盐酸 b.MgCl2溶液
c.BaCl2溶液 d.Ba(OH)2溶液
在验证的过程中,一定需要进行的操作是________(填字母序号)。
a.萃取 b.洗涤 c.过滤 d.分馏
③若白色固体X为第Ⅲ种组成,下列实验方案中不能测定其中NaHCO3质量分数的是________(填字母序号)。
a.取m g X与足量Ba(OH)2溶液充分反应,过滤,洗涤,烘干得n g固体
b.取m g X与足量盐酸充分反应,加热,蒸干,灼烧得n g固体
c.取m g X充分加热,减重n g
d.取m g X与足量稀硫酸充分反应,逸出的气体被足量碱石灰吸收,增重n g
④若白色固体X的质量为7.0 g,则X的组成为________(填Ⅰ、Ⅱ、Ⅲ或Ⅳ)。
答案 (1)①水沿导管由广口瓶进入烧瓶
②广口瓶中的长导管口有气泡产生
(2)Na2CO3 NaHCO3
①5.85 ②cb c ③d ④Ⅲ
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A的结构简式为:

(1)A与过量的NaOH溶液反应时,A与参加反应的NaOH的物质的量之比是 。
(2)A与新制Cu(OH)2反应时, A与被还原的Cu(OH)2的物质的量之比是 。1molA最多能消耗 mol Cu(OH)2。
(3)A与过量的NaHCO3反应时,A与NaHCO3的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)____HCl(浓)+____MnO2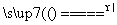 ____Cl2↑+____MnCl2+____H2O
____Cl2↑+____MnCl2+____H2O
(2)____Cu+____HNO3(稀)===____Cu(NO3)2+____NO↑+____H2O
(3)____KI+____KIO3+____H2SO4===____I2+____K2SO4+____H2O
(4)____MnO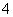 +____H++____Cl-===____Mn2++____Cl2↑+____H2O
+____H++____Cl-===____Mn2++____Cl2↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O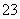 +O2+xOH-===Fe3O4↓+S4O
+O2+xOH-===Fe3O4↓+S4O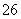 +2H2O。请回答下列问题。
+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是____________。
(2)反应的化学方程式中x=____ ____。
____。
(3)每生成1 mol Fe3O4,反应转移的电子为________mol,被Fe2+还原的O2的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
(2013·新课标全国卷Ⅱ,27)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:
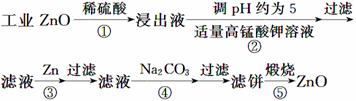
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
(2)反应③的反应类型为____________,过滤得到的滤渣中,除了过量的锌外还有______________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是________________。
(4)反应④中产物的成分可能是ZnCO3·xZn(OH)2,取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,则x等于__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.02 mol KMnO4固体加热一段时间后,收集到a mol甲气体,在反应后的残留固体中加入足量的浓盐酸,继续加热,又收集到b mol乙气体,设此时Mn元素全部以Mn2+存在于溶液中,则下列说法正确的是 ( )
A.甲、乙均为无色无味的气体
B.a的最大值为0.02
C.b的最小值为0.01
D.a+b的 最小值为0.04
最小值为0.04
查看答案和解析>>
科目:高中化学 来源: 题型:
在钢铁腐蚀过程中,下列五种变化可能发生的是
①Fe2+转化为Fe3+ ②O2被还原 ③产生H2 ④Fe(OH)3失水形成Fe2O3·H2O ⑤杂质碳被氧化
A.只有①和② B.只有②③④ C.①②③④ D.①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com