
【题目】有机物M的相对分子质量不超过150,经测定M具有下列性质:
①能燃烧,燃烧产物只有CO2和H2O
②M与醇或羧酸在浓硫酸存在下均能生成有香味的物质
③在一定条件下,M能发生分子内脱水反应,其生成物与溴水混合,溴水褪色
④0.1molM与足量NaHCO3溶液反应产生4.48L(标准状况下)气体
下列物质与M互为同系物的是( )
A.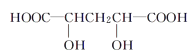 B.
B.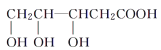
C.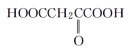 D.
D.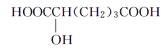
【答案】D
【解析】
①能燃烧,燃烧产物只有CO2和H2O,一定含有C、H元素,可能含有O元素;
②M与醇或羧酸在浓硫酸存在下均能生成有香味的物质,分子中含有-OH、-COOH;
③在一定条件下,M能发生分子内脱水反应,其生成物与溴水混合,溴水褪色,羟基的邻碳上有H;
④0.1molM与足量NaHCO3溶液反应产生4.48L(标准状况下)气体,即为0.2mol二氧化碳,分子中含有两个-COOH。
由分析可知:M分子中含有-OH、两个-COOH,M相对分子质量小于150,假设分子中含有两个-OH、两个-COOH,150-45×2-17×2=26,26可能有两CH,分子结构为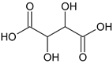 ,但该分子的相对分子质量等于于150,与题意不符,故M分子只有一个-OH、两个-COOH,D符合,故选D。
,但该分子的相对分子质量等于于150,与题意不符,故M分子只有一个-OH、两个-COOH,D符合,故选D。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在一定条件下可转化为B(如下图所示),下列说法正确的是
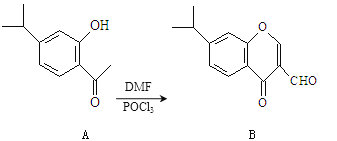
A.分子A中所有碳原子均位于同一平面
B.用FeCl3溶液可检验物质B中是否混有A
C.物质B既能发生银镜反应,又能发生水解反应
D.1mol B最多可与5mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体的叙述正确的是( )
A.![]() 苯环上的一氯取代物有5种
苯环上的一氯取代物有5种
B.丁烷(C4H10)的二氯取代物最多有4种
C. 和
和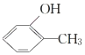 互为同分异构体
互为同分异构体
D.菲的结构简式为![]() ,其一硝基取代物有10种
,其一硝基取代物有10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为氯气与金属钠反应设计了如下装置与操作以替代相关的课本实验。实验操作:钠与氯气反应的装置作如下图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是( )
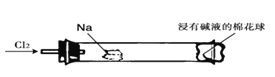
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 若在棉球外沿滴一滴淀粉碘化钾溶液,据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是制造新型信息材料的中间体,B是制备血管紧张素抑制剂卡托普利的原料,它们有如下的转化关系:

试回答下列问题:
(1)B的名称是______________,C含有的官能团名称是_____________。
(2)C→E的反应类型是_____________,C→F的反应类型是______________。
(3)A的结构简式为____________。
(4)写出与F具有相同官能团的F的所有同分异构体_____________(填结构简式)
(5)已知![]() ,请以2一甲基丙醇和甲醇为原料,设计制备有机玻璃(聚甲基丙烯酸甲酯)的合成路线.合成路线流程图示例如下:___________________
,请以2一甲基丙醇和甲醇为原料,设计制备有机玻璃(聚甲基丙烯酸甲酯)的合成路线.合成路线流程图示例如下:___________________![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(含氧化铝、氧化铁)制取金属铝的生产过程如下框图

请回答下列问题:
(1)纯净的氧化铝俗称____________,属于____________晶体。写出铝土矿与氢氧化钠溶液反应的离子方程式_______________。
(2)沉淀C的化学式为______,该物质除了用于金属冶炼以外,还可用作______________。电解熔融的氧化铝时,物质α是______,其作用是_________________。
(3)在实验室中欲从溶液E中得到较纯净的固体NaOH,需要进行的操作顺序是:_______、趁热过滤、____、__________。
(4)生产过程中,可以循环使用的物质有四种,除NaOH、H2O、CaO、CO2。其中NaOH中含有的化学键是______、________(如有共价键须标明极性还是非极性)。CaO、CO2的电子式分别为_____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应方程式如下,完成相应问题
___Fe3++___SO2+___H2O→___Fe2++___SO42-+___H+
(1)配平上述反应方程式并标出电子转移的方向和数目__________。
(2)反应中氧化剂为________,还原剂为________。
(3)反应中,所得氧化产物和还原产物的物质的量之比为_____________。
(4)反应过程中,溶液颜色由_______变为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
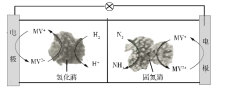
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将12.8g铜片加入到100mL一定浓度的硝酸溶液中,铜片完全溶解,产生NO和NO2的混合气体4.48L(标准状况下);若向反应后的溶液中加入400mL 2mol/LNaOH溶液,能使溶液中的Cu2+恰好完全沉淀.下列说法不正确的是![]()
![]()
A.铜片与硝酸反应过程中转移电子0.4mol
B.反应后溶液中剩余![]() 的物质的量为0.4mol
的物质的量为0.4mol
C.混合气体中NO和![]() 的体积之比为1:1
的体积之比为1:1
D.原硝酸溶液的物质的量浓度为10mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com