
 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.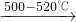 2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.
2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.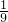 ,求该反应条件下混合气体的平均式量?
,求该反应条件下混合气体的平均式量?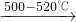 2BaO2
2BaO2 =15.3吨
=15.3吨 =2.117g,20℃时,Ba(OH)2饱和溶液的质量分数为
=2.117g,20℃时,Ba(OH)2饱和溶液的质量分数为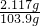 =0.02,
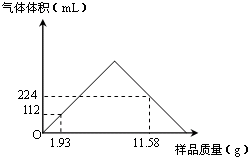
=0.02,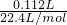 =0.005mol,根据碳原子守恒可知碳酸钡的物质的量为0.005mol,故11.58g混合物中含有的碳酸钡的物质的量为0.005mol×
=0.005mol,根据碳原子守恒可知碳酸钡的物质的量为0.005mol,故11.58g混合物中含有的碳酸钡的物质的量为0.005mol×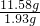 =0.03mol,故11.58g样品中BaCO3的质量为0.03mol×197g/mol=5.91g,
=0.03mol,故11.58g样品中BaCO3的质量为0.03mol×197g/mol=5.91g,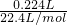 =0.01mol,故生成二氧化碳消耗的盐酸的物质的量为0.01mol×2=0.02mol,与氢氧化钡反应消耗的盐酸的物质的量为0.08L×1mol/L-0.02mol=0.06mol,故氢氧化钠晶体的物质的量为0.06mol×
=0.01mol,故生成二氧化碳消耗的盐酸的物质的量为0.01mol×2=0.02mol,与氢氧化钡反应消耗的盐酸的物质的量为0.08L×1mol/L-0.02mol=0.06mol,故氢氧化钠晶体的物质的量为0.06mol× =0.03mol,故0.03×(171+18n)=5.57,解得n=1,
=0.03mol,故0.03×(171+18n)=5.57,解得n=1, =2mol,故混合物水的物质的量为9mol-1mol-2mol=6mol,故混合气体的平均相对分子质量为
=2mol,故混合物水的物质的量为9mol-1mol-2mol=6mol,故混合气体的平均相对分子质量为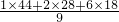 =23.11,
=23.11, ,故混合气体中二氧化碳与CO的物质的量之比为0.94×
,故混合气体中二氧化碳与CO的物质的量之比为0.94× :0.02=47:3,转化的甲烷物质的量为2.0×106 mol×95%,由碳元素守恒可知,二氧化碳、CO的总的物质的量为2.0×106 mol×95%,故二氧化碳为2.0×106 mol×95%×
:0.02=47:3,转化的甲烷物质的量为2.0×106 mol×95%,由碳元素守恒可知,二氧化碳、CO的总的物质的量为2.0×106 mol×95%,故二氧化碳为2.0×106 mol×95%×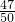 ,CO物质的量为2.0×106 mol×95%×
,CO物质的量为2.0×106 mol×95%× ,结合方程式可知生成BaS的物质的量为2.0×106 mol×95%×
,结合方程式可知生成BaS的物质的量为2.0×106 mol×95%×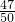 +2.0×106 mol×95%×
+2.0×106 mol×95%× ×
×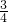 =2.0×106×95%×
=2.0×106×95%× mol,故生成BaS的质量为2.0×106×95%×
mol,故生成BaS的质量为2.0×106×95%× mol×169g/mol=316.28×106 g=316.28吨,
mol×169g/mol=316.28×106 g=316.28吨, 计算二氧化碳的物质的量,根据碳原子守恒计算碳酸钡的物质的量,根据定组成计算11.58g混合物中含有的碳酸钡的物质的量,进而根据m=nM计算碳酸钡的质量;
计算二氧化碳的物质的量,根据碳原子守恒计算碳酸钡的物质的量,根据定组成计算11.58g混合物中含有的碳酸钡的物质的量,进而根据m=nM计算碳酸钡的质量; 计算二氧化碳的物质的量,计算生成二氧化碳消耗的盐酸的物质的量,进而计算与氢氧化钡反应消耗的盐酸的物质的量,可得氢氧化钠晶体的物质的量,进而计算氢氧化钡晶体中n的值;
计算二氧化碳的物质的量,计算生成二氧化碳消耗的盐酸的物质的量,进而计算与氢氧化钡反应消耗的盐酸的物质的量,可得氢氧化钠晶体的物质的量,进而计算氢氧化钡晶体中n的值; =
= 计算;
计算; ,据此计算混合气体中二氧化碳与CO的物质的量之比,根据转化的甲烷计算二氧化碳、CO的物质的量,结合方程式计算BaS的物质的量,进而计算其质量.
,据此计算混合气体中二氧化碳与CO的物质的量之比,根据转化的甲烷计算二氧化碳、CO的物质的量,结合方程式计算BaS的物质的量,进而计算其质量.

 阅读快车系列答案
阅读快车系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com