
某稀硫酸和硝酸的混合溶液200 mL,
分成两份。向其中一份逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO)。向另一份逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如下图所示。

(1)第二份溶液中最终溶质为 ;
(2)OA段产生的气体是 (填化学式),BC段产生的气体是 (填化学式),AB段的反应为 ;
(3)原混合酸中HNO3的物质的量为 mol,H2SO4的物质的量浓度应为 mol/L。
【知识点】物质之间的反应和图像的分析
【答案解析】(1)FeSO4
(2)NO H2 Fe +2Fe 3+=3Fe2+
(3)0.4 4
解析:当在溶液中加入铁粉时,铁首先应该与硝酸反应生成Fe3+,即OA段产生的是NO;当硝酸完全反应时,铁与Fe 3+反应生成Fe 2+,即AB段发生的反应为Fe +2Fe 3+=3Fe2+;当Fe 3+完全反应后再加入铁粉,铁与溶液中的H+反应,即BC段产生的气体是H2;根据分析得到第二份溶液中最终溶质为FeSO4。
根据图示可以看出溶液中的H+足够,所以在OA段NO3—完全反应,
Fe+4H++NO3—= Fe3++NO+H2O ①
n(Fe)=11.2g/56g/mol=0.2mol= n(NO3—)=n(HNO3),故原混合酸中HNO3的物质的量为0.4mol;
BC段发生的是Fe+2H+= Fe2+ +H2 ②
n(H+)= 2n(Fe)=2×5.6g/56g/mol=0.2mol,
在①中由硫酸提供的n(H+)=3 n(NO3—)= 0.6mol,故第二份溶液中n(H+)总=0.8mol,n(H2SO4)= 0.4mol,则原溶液中n(H2SO4)= 0.8mol,H2SO4的物质的量浓度应为0.8mol /200 mL =4mol/L。
【思路点拨】①此溶液分成了两等分,②硝酸根在酸性的条件下提供氧化性是本题考查的重点,是易错题,综合性强。


科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA
B.l mol Fe(NO3)3与足量HI溶液反应时转移的电子数为3NA
C.1 mol Na2O2固体中含离子总数为4NA
D.常温下,1 mol Fe与过量浓HNO3反应,转移电子的数目为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是 ( )
A.同周期元素中X的金属性最强 B.同周期元素中Y的最高价含氧酸的酸性最强
C.原子半径X>Y,离子半径X+>Z2- D.同族元素中Z的氢化物稳定性最高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化,形成致密的氧化膜 |
| C | 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 该溶液中存在NH4+ |
| D | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在下图所示的物质转化关系中(反应条件和部分生成物未全部列出),X物质可以来自于海洋中,A、B为常见气体单质,B为黄绿色气体,I、L为常见的金属单质,G为红褐色物质。请回答下列问题:

(1)X化学式为 。 (2)C化学式为 。
(3)反应①的离子方程式为 。
(4)反应②的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据如图提供的信息,下列所得结论不正确的是( )
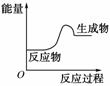
A.该反应为吸热反应
B.该反应一定有能量转化成了化学能
C.反应物比生成物稳定
D.因为生成物的总能量高于反应物的总能量,所以该反应不需要加热
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)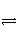
 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A.升高温度,正反应速率增加,逆反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com