
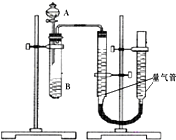
 甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O)
甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O)| 序号 | A溶液 | B溶液 |
| ① | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
| ② | 2ml 0.1mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
| ③ | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液和少量MnSO4 |
| 实验编号 | 1 | 2 | 3 | 4 |
| 水/ml | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/ml | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/ml | 5 | 5 | 10 | 10 |
| 时间/s | 40 | 20 | 10 | --- |
分析 (1)根据实验①②、①③中不同的物理量判断该实验目的;
(2)无论避免影响测定结果,分液漏斗中的A溶液不能逐滴加入;
(3)使装置内外形成气压差是气密性检查的常用手段;
(4)探究浓度对反应速率的影响时,溶液的总体积都为20mL,据此判断X值;由于4号实验中高锰酸钾过量,则溶液没有褪色.
解答 解:(1)根据表中数据可知,实验①②探究的是浓度对反应速率的影响,实验①③探究的是催化剂对反应速率的影响,所以该实验的目的是探究温度、催化剂对反应速率的影响,故答案为:草酸浓度和催化剂;
(2)为了避免实验误差,实验过程中分液漏斗中的溶液A必须一次性加入,不能逐滴加入,
故答案为:一次性;
(3)实验结束后读数前需要移动量气管,使两个量气管的液面相平,其作用是使两个量气管的压强相等,避免产生压强差,影响测定结果,
故答案为:移动量气管,使两个量气管的液面相平;
(4)为了探究KMnO4与H2C2O4浓度对反应速率的影响,实验1-4中溶液的总体积应该为20,则X=20-10-5=5;根据反应2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O可知,10mL酸性高锰酸钾需要消耗10mL草酸溶液,所以实验4中高锰酸钾过量,导致溶液没有褪色,
故答案为:A;KMnO4溶液过量.
点评 本题考查了探究浓度度、催化剂对反应速率的影响等知识,题目难度中等,注意掌握影响化学反应速率的因素,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验、化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含有大量NH4+的溶液:Mg2+、S2-、OH-、I- | |
| C. | 通有足量NO2的溶液:K+、Na+、SO32-、AlO2- | |
| D. | 强酸性溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
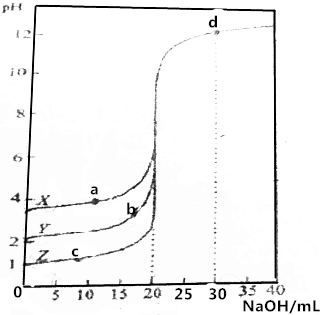 用0.1000mol•L-1的NaOH溶液分别滴定0.1000mol•L-1、20.00mLX、Y、Z三种酸溶液.溶液pH与加入NaOH体积之间的关系如图所示,下列说法错误的是( )
用0.1000mol•L-1的NaOH溶液分别滴定0.1000mol•L-1、20.00mLX、Y、Z三种酸溶液.溶液pH与加入NaOH体积之间的关系如图所示,下列说法错误的是( )| A. | Z为一元强酸 | |
| B. | d点的c(OH-)为0.02000mol•L-1 | |
| C. | a、b、c中b点的阴离子的物质的量浓度最大 | |
| D. | X、Y为一元弱酸,且其电离常数:Ka(x)<Ka(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 燃烧是发光、发热的化学反应 | B. | 燃烧必须有02参加 | ||
| C. | 燃烧必须有H20参加 | D. | 燃烧一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol•L-1的HCl标准溶液进行中和滴定(用甲基橙作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用0.1000mol•L-1的HCl标准溶液进行中和滴定(用甲基橙作指示剂).| 实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol•L-1HCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
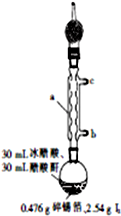 四碘化锡(SnI4)是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:
四碘化锡(SnI4)是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
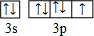 ,R基态原子的外围电子排布式为3d104s1.
,R基态原子的外围电子排布式为3d104s1.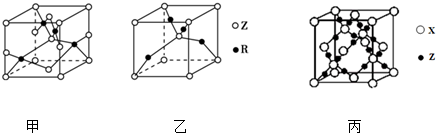
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com