
【题目】已知钍![]() 的原子可发生下列放射性变化:
的原子可发生下列放射性变化: ![]() →
→![]() +
+ ![]() ,生成的X是与Mg同主族的一种元素的原子,下列对X的推断不正确的是
,生成的X是与Mg同主族的一种元素的原子,下列对X的推断不正确的是
A. X元素位于第六周期 B. X的氢氧化物是一种强碱
C. X的碳酸盐难溶于水 D. X的最高化合价为+2价
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】在Na2SO4 和 Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,SO42-浓度为0.3mol/L,则混合溶液中Na+的浓度为
A.0.15mol/L B.0.45mol/L C.0.6mol/L D.0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,X、Y、Z、R为短周期元素,其中Y元素的原子最外层电子数是其内层电子数的3倍。下列说法正确的是
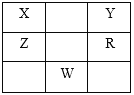
A. 原子半径大小关系为: R> Y > X
B. X有多种同素异形体,而Y不存在同素异形体
C. 根据元素周期律,可以推测W元素的单质具有半导体特性,W2Y3具有氧化性和还原性
D. ZY2晶体熔化、液态RY3气化均需克服分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“化学与生活”的说法错误的是( )
A. 硫酸钡可用作钡餐 B. 纯碱可用于去油污
C. 明矾可用于水的消毒、杀菌 D. 醋可用于除去暖水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。图2中,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
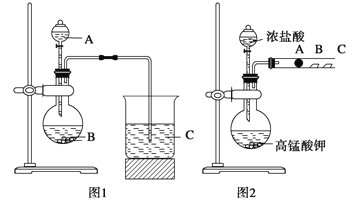
(1)甲同学实验(如图1)中选用的三种物质名称分别为:______________________________;
(2)乙同学实验(如图2)中:A处反应的离子方程式为:_______________________________;
B处的实验现象为:___________________________;
该实验不能完全证明卤素性质的递变规律,请简述原因:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物的合成与结构修饰是制备具有特殊功能材料的重要过程。下图是合成具有特殊功能高分子材料W(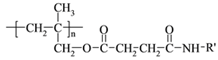 )的流程:
)的流程:
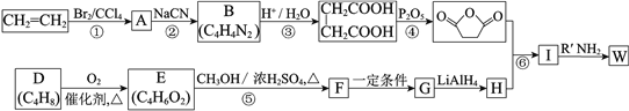
已知:(R、R1、R2代表烃基)
I、![]()
![]() RCH2OH
RCH2OH
II、![]()
⑴反应①的反应类型是_______________。
⑵反应②是取代反应,其化学方程式是___________________________________________。
⑶D的核磁共振氢谱中有两组峰且面积之比是1:3,不存在顺反异构。D的结构简式是______。
⑷反应⑤的化学方程式是__________________________________________________。
⑸G的结构简式是__________________。
⑹反应⑥的化学方程式是__________________________________________________。
⑺工业上也可用![]() 合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,
合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,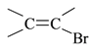 不易发生取代反应)__________________
不易发生取代反应)__________________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
①0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO![]()
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-、NO3-
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-
A.②④⑥ B.②⑥ C.② D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com