
| A. | 硝酸浓度越大消耗的硝酸越少,产生的有毒气体也越少 | |
| B. | 反应中转移的电子总数稀硝酸少 | |
| C. | 试管内壁上的铜用浓硝酸除好,因反应速率快 | |
| D. | 两者用排水法收集的气体的体积相同 |
分析 根据3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O、Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O、3NO2+H2O═2HNO3+NO来解答.
解答 解:相同质量的铜分别与足量的稀硝酸和浓硝酸完全反应,发生3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O、Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,
A.等量的Cu与酸反应,浓硝酸消耗的多,生成有毒气体多,故A错误;
B.等量的Cu与酸反应,生成Cu(NO3)2的物质的量相同,由Cu元素的化合价变化可知转移电子相同,故B错误;
C.等量的Cu与酸反应,消耗的稀硝酸少,则试管内壁上的铜用稀硝酸除好,故C错误;
D.因3NO2+H2O═2HNO3+NO,最终收集气体均为NO,由电子守恒可知,收集NO的体积相等,故D正确;
故选D.
点评 本题考查硝酸的性质及应用,为高频考点,把握发生的氧化还原反应、实验评价为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:选择题
| A. | 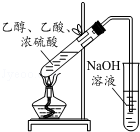 实验室中制取少量的乙酸乙酯 | |
| B. | 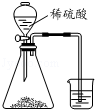 比较硫、碳、硅三种元素的非金属性强弱 | |
| C. | 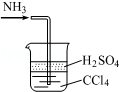 处理尾气 | |
| D. | 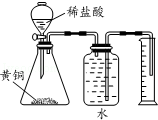 测定黄铜(Cu、Zn合金)中Zn 的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取30mL溶液 | B. | 用四氯化碳萃取碘水中的碘 | ||
| C. | 用托盘天平称取2.5g固体 | D. | 用温度计代替玻璃棒搅拌溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 面粉-淀粉 | B. | 牛肉-蛋白质 | C. | 桔子-维生素 | D. | 梅子蜜饯-防腐剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个原子之间的相互作用叫做化学键 | |
| B. | 相邻原子之间的相互作用叫做化学键 | |
| C. | 一切物质中都存在化学键 | |
| D. | 破坏化学键一定要消耗能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
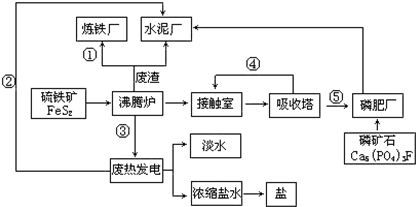
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 很多水果具有酸味,因此在化学上称为酸性食物 | |
| B. | 为增强婴儿的食欲,应在婴儿食品中多加着色剂 | |
| C. | 多吃含钙丰富的豆腐可预防骨质疏松 | |
| D. | 为摄取足够的蛋白质,应多吃肉、少吃豆制品 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
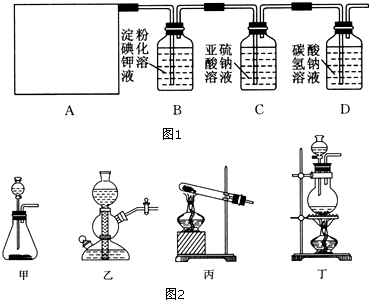
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com