
【题目】下列事实,能用勒夏特列原理解释的是( )
A. H2、I2、HI平衡混和气加压后颜色变深 B. 实验室中常用排饱和食盐水的方法收集Cl2
C. 合成氨控制在500 ℃左右的温度 D. SO2催化氧化成SO3的反应,往往需要使用催化剂
【答案】B
【解析】
A.H2、I2、HI三者的平衡,增大压强平衡不移动,但浓度增大,则颜色加深,不能用勒沙特列原理解释,选项A不选;B.氯化钠在溶液中完全电离,所以饱和食盐水中含有大量的氯离子,氯气溶于水的反应是一个可逆反应,Cl2+H2O![]() HClO+H++Cl-,由于饱和食盐水中含有大量的氯离子,相当于氯气溶于水的反应中增加了大量的生成物氯离子,根据勒夏特列原理,平衡向逆反应方向移动,氯气溶解量减小,所以可以勒夏特列原理解释,选项B选;C、合成氨反应为放热反应,采用500℃的温度,不利于平衡向正方向移动,主要是考虑催化剂的活性和反应速率,不能用勒夏特列原理解释,选项C不选;D、催化剂只改变化学反应速率不改变化学平衡,SO2催化氧化成SO3的反应,往往需要使用催化剂是为了提高反应速率,和平衡无关,选项D不选;答案选B。
HClO+H++Cl-,由于饱和食盐水中含有大量的氯离子,相当于氯气溶于水的反应中增加了大量的生成物氯离子,根据勒夏特列原理,平衡向逆反应方向移动,氯气溶解量减小,所以可以勒夏特列原理解释,选项B选;C、合成氨反应为放热反应,采用500℃的温度,不利于平衡向正方向移动,主要是考虑催化剂的活性和反应速率,不能用勒夏特列原理解释,选项C不选;D、催化剂只改变化学反应速率不改变化学平衡,SO2催化氧化成SO3的反应,往往需要使用催化剂是为了提高反应速率,和平衡无关,选项D不选;答案选B。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】(1)铅及其化合物可用于蓄电池,耐酸设备及 X 射线防护材料等。回答下 列问题:
①铅是碳的同族元素,比碳多 4 个电子层。铅的原子结构示意图为_____;铅的最高价氧化物对应水化物的酸性比碳酸的______(填“强”或“弱”)。
②PbO2 与浓盐酸共热生成黄绿色气体,反应的化学方程式为_____。
③铅蓄电池放电时的正极反应式为_____ ,当电路中有 2mol 电子转移时,理论上两电极质量变化的差为_____g。
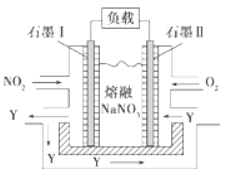
(2)NO2、O2 和熔融 NaNO3 可制作燃料电池,其原理见下图,石墨Ⅰ为电池的_____极;该电池在使用过程中石墨Ⅰ电极上生成氧化物 Y,其电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2(g)+I2(g) ![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | c |
下列判断不正确的是
A. HI的平衡浓度:a=b>0.004,c=0.008 B. 平衡时,H2的转化率:丁>甲
C. 平衡时,乙中H2的转化率大于20% D. 丙中条件下,该反应的平衡常数K=0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 用浓盐酸分别和KMnO4、KClO3反应制备l mol氯气,转移的电子数均为2NA
D. 5.6gFe粉与足量S粉加热充分反应转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个容积不变的密闭容器中充入一定量A和B,发生如下反应:x A(g) +2B(s)![]() y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g); △H <0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
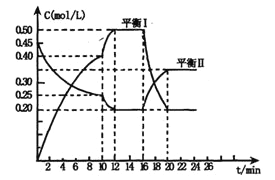
(1)用A的浓度变化表示该反应0~10min内的平均反应速率v(A)=________;
(2)根据图示可确定x:y=_______________;
(3)0~l0min容器内压强_______________(填“变大”,“不变”或“变小”)
(4)推测第l0min引起曲线变化的反应条件可能是____________;第16min引起曲线变化的反应条件可能是____________;
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。下列说法不正确的是

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及极性键的断裂与生成
C. 氧化剂与还原剂的物质的量之比为1∶3
D. 原料气N2可通过分离液态空气获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)![]() 2NH3(g)。该可逆反应达到平衡的标志是________。
2NH3(g)。该可逆反应达到平衡的标志是________。
A.3v正(H2)=2v逆(NH3) B.单位时间生成m mol N2的同时生成3m mol H2
C.容器内的总压强不再随时间而变化 D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取合成氨的原料气氢气。某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2 L的恒容密闭容器中测得如下表所示数据。请回答下列问题:
时间/min | CH4/mol | H2O/mol | CO/mol | H2/mol |
0 | 0.40 | 1.00 | 0 | 0 |
5 | a | 0.80 | c | 0.60 |
7 | 0.20 | b | 0.20 | d |
分析表中数据,判断5 min时反应是否处于平衡状态?______(填“是”或“否”),前5 min反应的平均反应速率v(CH4)=____________________。
(3)恒温恒容下,将2 mol 气体A和2 mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g) xC(g)+2D(s),2 min后反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol/L。
①x=________。
②A的转化率与B的转化率之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于二氧化硫的下列叙述中,正确的是( )
A.能使含有酚酞的氢氧化钠溶液褪色,体现了二氧化硫的漂白性
B.二氧化硫能使石蕊溶液先变红色再褪色,体现了二氧化硫的酸性和漂白性
C.二氧化硫、氯气都能使品红溶液褪色,但原理不同
D.二氧化硫通入足量氯化钙溶液,能生成白色的亚硫酸钙沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气是一种宝贵的自然资源,下列有关说法正确的是( )
A.稀有气体约占空气质量的0.03%
B.空气质量指数级别越大,空气质量越好
C.氮气常温下化学性质稳定,可用于生产氮肥
D.氦气可用于填充探空气球
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com