
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 甲烷的球棍模型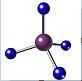 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 四氯化碳分子的电子式: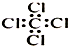 |
分析 A.含有羟基最长的碳链有3个碳原子,有1个甲基在2号碳上;
B.球棍模型中短线表示化学键、小球表示原子,表现分子中原子的连接、成键方式、空间结构;
C.结构式是表示用元素符号和短线表示化合物(或单质)分子中原子的排列和结合方式的式子;
D.四氯化碳的电子式中漏掉了Cl原子的3对未成键电子对.
解答 解:A.(CH3)3COH中含有羟基最长的碳链有3个碳原子,有1个甲基在2号碳上,名称为:2-甲基-2-丙醇,故A错误;
B.甲烷分子式为CH4,C原子形成4个C-H,为正四面体结构,碳原子半径大于氢原子半径,球棍模型为: ,故B正确;
,故B正确;
C.CH3CHO为乙醛的结构简式,乙醛的结构式为: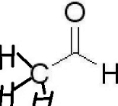 ,故C错误;
,故C错误;
D.氯原子未成键的孤对电子对未标出,四氯化碳正确的电子式为 ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及电子式、结构简式、球棍模型、有机物命名等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中,每生成1molAlN需转移6mol电子 | |
| C. | AlN属于离子化合物,其中氮元素的化合价为+3 | |
| D. | AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O═NaAlO2+NH3↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上合成氨,及时分离出产物氨有利于提高氮气的转化率 | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 B
B D
D .写出D→E的反应的化学方程式
.写出D→E的反应的化学方程式 +CH3OH$→_{△}^{浓硫酸}$
+CH3OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com