
 ;
;分析 (1)氯乙烷在NaOH溶液中可发生取代反应生成乙醇和氯化钠;
(2)丙烯发生加聚反应生成聚丙烯;
(3)2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水.
解答 解:(1)氯乙烷和氢氧化钠溶液加热发生取代反应生成乙醇和氯化钠,反应的化学方程式为CH3CH2Cl+NaOH$\stackrel{△}{→}$NaCl+CH3CH2OH,
故答案为:CH3CH2Cl+NaOH$\stackrel{△}{→}$NaCl+CH3CH2OH;
(2)丙烯中含C=C,发生加聚反应生成聚丙烯,化学方程式为 ,
,
故答案为: ;
;
(3)2-溴丙烷在氢氧化钠的醇溶液中发生消去反应生成丙烯、溴化钠和水,反应的化学方程式为:CH3-CHBr-CH3+NaOH$→_{△}^{氢氧化钠}$CH3-CH=CH2↑+NaBr+H2O;
故答案为:CH3-CHBr-CH3+NaOH$→_{△}^{氢氧化钠}$CH3-CH=CH2↑+NaBr+H2O.
点评 本题考查了化学方程式的书写,侧重考查有机化学反应方程式的书写,明确有机物的结构特点是解题关键,题目难度不大.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | N2、NO2、粉尘、煤烟 | B. | CO2、O2、氮的氧化物、碳氢化合物 | ||
| C. | Cl2、N2、煤烟、氮的氧化物 | D. | H2S、SO2、粉尘、煤烟、氮的氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
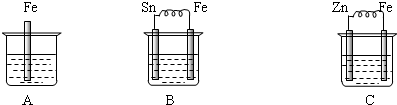
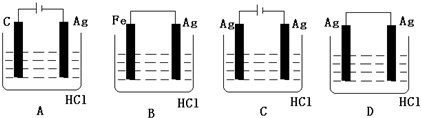
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH━CH一CH3 | B. | CH3-C≡CH | C. | CH≡CH | D. | CH3-C≡C-CH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
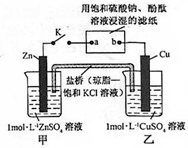
| A. | 片刻后甲池中c(SO42-)增大 | B. | 电子沿 Zn→a→b→Cu 路径流动 | ||
| C. | Cu 电极上发生还原反应 | D. | 片刻后可观察到滤纸b点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CHBr属于卤代烃 | |
| B. | 卤代烃密度都大于水 | |
| C. | 卤代烃都会水解生成醇 | |
| D. | 卤代烃都能和NaOH醇溶液发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 若定容时,加水越过刻度线,则所配得溶液的浓度偏高 | |
| B. | 若忘记将洗涤液加入容量瓶,则所配得溶液的浓度偏低 | |
| C. | 若定容后摇匀液面低于刻度线,再加水至刻度线,所得溶液浓度为0.1mol•L -1 | |
| D. | 若定容时俯视刻度线,则所配得溶液浓度偏高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com