



 kJ/mol
kJ/mol kJ/mol。
kJ/mol。

科目:高中化学 来源:不详 题型:单选题
| A.C + CO2=2CO | B.C + O2=CO2 |
| C.2C + O2= 2CO | D.C + CuO=CO2 + Cu |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0 |
| C.破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为吸热反应 |
| D.ΔH的大小与热化学方程式的计量数无关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝热反应 | B.铝与盐酸反应 |
| C.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 | D.灼热的炭与CO2反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)="===" CO2(g)+H2(g)ΔH =" -41.2" kJ·mol-1 |
| B.H2的燃烧热为241.8 kJ·mol-1 |
| C.H2(g)转变成H2O(g)的化学反应一定要释放能量 |
| D.根据②推知反应H2(g)+1/2O2(g)="===" H2O(l)ΔH > -241.8 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.需要加热方能发生的反应一定是吸热反应 |
| B.放热的反应在常温下一般容易发生 |
| C.反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 |
| D.吸热反应在一定的条件下也能发生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应热就是反应中放出的热量 |
| B.当反应放热时ΔH>0,反应吸热时ΔH<0 |
| C.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,ΔH为“-” |
| D.一个化学反应中,生成物总键能大于反应物的总键能时,反应吸热,ΔH为“+” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
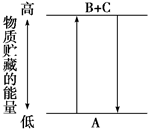
| A.A→B+C和B+C→A两个反应吸收或放出的能量数值不相等 |
| B.A→B+C是放热反应 |
| C.A具有的能量高于B和C具有的能量总和 |
| D.A→B+C是吸热反应,则B+C→A必然是放热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.干冰升华要吸收大量的热,这就是化学反应中的吸热反应 |
| B.酒精常被用作酒精灯和内燃机中的燃料,说明酒精燃烧是放热反应 |
| C.木炭常温下不燃烧,加热才能燃烧,但木炭燃烧是放热反应 |
| D.人们用氢氧焰焊接或切割金属,主要是利用了氢气和氧气化合时所放出的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com