
| A. | 沸点:正己烷>3-甲基戊烷>2-甲基丁烷 | |
| B. | 含氢量:乙烯>乙苯>乙炔 | |
| C. | 密度:苯>H2O>CCl4 | |
| D. | 相同质量的物质含共用电子对总数:乙烷>乙烯>乙炔 |
分析 A.烃类物质中,烃含有的C原子数目越多,相对分子质量越大,熔沸点越高,同分异构体分子中,烃含有的支链越多,熔沸点越小;
B.碳氢比小的氢的质量分数大;
C.苯的密度小于1g/mL、水的密度是1g/mL、四氯化碳的密度大于1g/mL;
D.乙烷分子中含共用电子对7,乙烯分子中含共用电子对6,乙炔分子中含共用电子对5,等质量物质均是其物质的量比较.
解答 解:A.己烷中含有6个C,3-甲基戊烷含有6个C,己烷没有支链,2-甲基丁烷含5个碳,所以沸点:正己烷>3-甲基戊烷>2-甲基丁烷,故A正确;
B.乙烯、乙苯、乙炔的碳氢比分别为:1:2;7:8:1:1,氢的质量分数:乙烯>乙苯>乙炔,故B正确;
C.苯的密度小于1g/mL、水的密度是1g/mL、四氯化碳的密度大于1g/mL,密度:苯<H2O<CCl4,故C错误;
D.相同质量的物质乙烷分子中含共用电子对7×$\frac{1}{30}$,乙烯分子中含共用电子对6×$\frac{1}{28}$,乙炔分子中含共用电子对5×$\frac{1}{26}$,相同质量的物质含共用电子对总数:乙烷>乙烯>乙炔,故D正确;
故选C.
点评 本题考查物质结构、物质物理性质、分子结构和共价键的计算、元素含量比较,注意规律的应用是解答本题的关键,要求学生学会归纳总结,题目难度中等.


科目:高中化学 来源: 题型:多选题
| X | Y | W | |
| Z |
| A. | 四种元素的单质中,W的氧化性最强 | |
| B. | Z元素的气态氢化物稳定性比W强 | |
| C. | Y元素的氧化物对应水化物的酸性一定比Z弱 | |
| D. | X、Z元素能形成化学式为XZ2的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol | B. | 小于0.15mol | C. | 0.15~0.3mol | D. | 0.15mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1mol CO2、CO的混合气中含有的碳原子数为NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 1mol氯气与足量的氢氧化钠溶液完全反应转移的电子数为2NA | |
| D. | 1L 1mol•L-1 CuCl2溶液中含有的氯离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 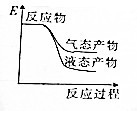 | B. | 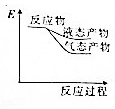 | C. | 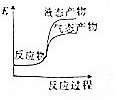 | D. | 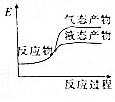 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯碱工业中,氢氧化钠在电解槽的阳极区产生 | |
| B. | 硫酸工业中,二氧化硫催化氧化使用催化剂,可增加二氧化硫的转化率 | |
| C. | 合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 | |
| D. | 接触法制硫酸中三氧化硫用水吸收制成浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤 | B. | 蒸发 | C. | 分液 | D. | 分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基中含有电子数为10NA | |
| B. | 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA | |
| C. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA | |
| D. | 50mL12mol•L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com