
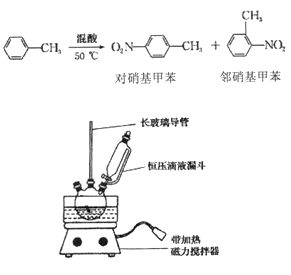
【题目】实验室制备一硝基甲笨(主要含邻硝基甲苯和对硝基甲苯)的反应原理、实验装
密度/(g·cm-3) | 沸点/℃ | 式量 | 溶解性 | |
甲苯 | 0.866 | 110.6 | 92 | 不溶于水,易溶于一硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 137 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 137 | 不溶于水,易溶于液态烃 |
实验步骤:
① 配制混酸,组装如图反应装置。取100 mL 烧杯,用10 mL 浓硫酸与30 mL 浓硝酸配
制混酸,加入恒压滴液漏斗中,把15 mL 甲苯(折合质量13.0g)加入三颈烧瓶中。
② 向室温下的甲苯中逐滴加混酸,边滴边搅拌,混合均匀。
③ 在50一60℃ 下发生反应,直至反应结束。
④ 除去混酸后,依次用蒸馏水和10% NaCO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
请回答下列问题:
(l)配制40mL 混酸的操作是________________
(2)装置中还缺少__________(填仪器名称)。如果温度超过60℃,将会有____(填物质名称)生成。
(3)分离粗产品和水的操作方法是__________
(4)产品用10% NaCO3溶液洗涤之后,再用蒸馏水洗涤,检验产品是否洗干净的操作是_______
(5)为了得到更纯净的硝基苯,还须先向液体中加入_______除去水,然后蒸馏,若最终得到产品的质量为13.70g,则一硝基甲苯的产率是________。
【答案】 分别取30 mL浓硝酸和10 mL浓硫酸,将30 mL浓硝酸倒入烧杯中,再慢慢沿烧杯内壁注入10 mL浓硫酸,边加边搅拌 温度计 二硝基甲苯或三硝基甲苯 分液 取最后一次洗涤液少许于试管中,滴加氯化钙溶液,无沉淀生成,则说明已洗净 CaO 70.8%
【解析】制备一硝基甲苯:先配制混合溶液(即混酸)共40mL,因反应液体沸点较低,加热时容易发生暴沸,所以在三颈瓶中加入沸石,然后加入15ml甲苯(易挥发沸点为110.6℃),再向三颈瓶中加入混酸,水浴(水的沸点100℃)目的能均匀加热,且便于控制反应速率,温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;两种一硝基化合物都为有机物,所以只能利用它们沸点的不同采用蒸馏的方法分离,经提纯最终得到纯净的一硝基甲苯.
(l)配制混合溶液时,操作流程与浓硫酸的稀释一样,分别量取10 mL浓硫酸和30mL的和浓硝酸,将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌,配制混合溶液(即混酸)共40mL;
(2)浴加热时需要控制温度50一60℃左右,应该有温度计测水浴温度,则装置中还缺少温度计;如果温度超过60℃,一硝基苯需要继续被硝化,有二硝基甲苯或三硝基甲苯生成;
(3)粗产品和水互不相溶,可通过分液漏斗进行分液分离;
(4)反应得到粗产品中有残留的硝酸及硫酸,用10%Na2CO3溶液洗涤除去粗产品中残留的酸,之后再用蒸馏水洗涤,如果晶体未洗净含有碳酸根离子,取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净;
(5)用蒸馏水洗涤,邻硝基甲苯中含有水,用无水CaO或CaCl2干燥,然后将较纯的一邻硝基甲苯进行蒸馏,得到邻硝基甲苯;由于15mL苯质量为13.0g,根据反应![]() +HNO3(浓)
+HNO3(浓)![]()
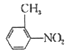 +H2O,可知硝基苯的质量=
+H2O,可知硝基苯的质量=![]() ≈19.36g,故硝基苯的产率为
≈19.36g,故硝基苯的产率为![]() ×100%=70.8%。
×100%=70.8%。


科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化性漂白剂。主要用于棉纺、亚麻、纸浆漂白、食品消毒、水处理、杀菌灭藻和鱼药制造。某化学兴趣小组对亚氯酸进行了研究,请回答下列问题。
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaC1。
(1)下列物质中与亚氯酸钠漂白原理相同的是_______。
A.H2O2 B.NaClO C.SO2 D.Al(OH)3胶体
(2)现利用下图所示装置(夹持装置省略)进行制取NaClO2晶体实验。
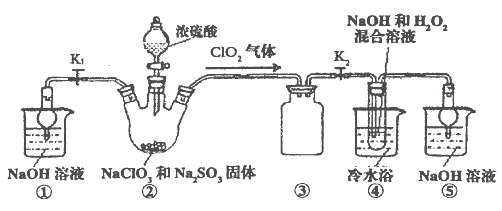
a.装置②中两种实验仪器的名称分别是_____________、___________。
b.装置②中产生ClO2的化学方程式为_________________________。
装置④中制备NaClO2的离子方程式为________________________。
c.装置③的作用是________________。
d.未反应完的ClO2在装置⑤中可被NaOH溶液吸收,生成的氧化产物与还原产物均为含氧酸盐,且二者的物质的量之比为1:1,请写出该反应的离子方程式______________________。
e.从装置④反应后的溶液获得NaClO2晶体的操作步骤如下:
①减压,55℃蒸发结晶;②趁热过滤;③___________;④低于60℃干燥,得到成品。
(3)用如下实验方案测定亚氯酸钠样品的纯度。
亚氯酸钠样品纯度测定实验用到的化学反应方程式为ClO2-+4I-+4H+=2H2O+2I2+Cl-、I2+2S2O32-=2I-+S4O62-
a.该测定实验用到的指示剂为_________________。
b.为测定亚氯酸钠样品纯度,需要用到下列实验数据中的___________(填写选项字母)
A.亚氯酸钠样品的质量(a g)
B.过量的碘化钾晶体的质量(b g)
C.稀硫酸的浓度(cmol/L)和体积(D mL)
D.指示剂的加入量(d mol)
E.标准液的浓度(e mol/L)和消耗体积(VmL)
用上述选定的数据表示出样品中NaC1O2 质量分数____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)恒温恒容下,在某密闭容器中充入CO(NH2)2和H2O,在120℃、催化剂作用下发生反应:CO(NH2)2 (s) + H2O(g)![]() 2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。
2 NH3(g)+CO2(g) △H >0。该反应的化学平衡常数的表达式K= 。
关于该反应的下列说法正确的是
A.混合气体的平均相对分子质量不再改变,可以作为化学平衡到达的标志
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.降低温度使CO(NH2)2的转化率增大
D.达到平衡后,再充入少量H2O,重新达到平衡,H2O的转化率会减小
(2)一定条件下,某密闭容器中充入等物质的量的NH3和CO2,发生反应:CO2(g) +2NH3(g)![]() CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的体积分数[φ(NH3)]随时间变化关系如图所示。
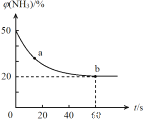
则a点的正反应速率V正(CO2)_________ b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mLNaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应,下图表示加入的混合物的质量和产生气体的体积(标准状况)关系。
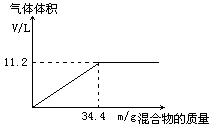
(1)试计算NaOH溶液的物质的量浓度。
(2)当NaOH溶液的体积为140mL,固体混合物的质量为51.6g,充分反应后,生成气体的体积(标准状况)为多少升?
(3)当NaOH溶液的体积为180mL,固体混合物的质量仍为51.6g,充分反应后,生成气体的体积(标准状况)为多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态化合物AB会发生微弱的自身电离,电离方程式为AB![]() A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A.c(A+)随温度升高而降低
B.在35 ℃时,c(A+)>c(B-)
C.AB的电离程度(25 ℃)>(35 ℃)
D.AB的电离是吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:2X(g)![]() Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为____________ mol·L-1·min-1。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5 mol·L-1·min-1;乙:v(Y)=2 mol·L-1·min-1;丙:v(Z)=4.5 mol·L-1·min-1;丁:v(X)=0.075 mol·L-1·s-1。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)______ ______。
(3)若向达到(1)的平衡体系中充入氦气,则平衡__________(填“向左”、“向右”或“不”)移动;若从达到(1)的平衡体系中移走部分Y气体,则平衡____________(填“向左”、“向右”或“不”)移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5 mol X气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较( )
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则:a、b、c应该满足的关系为___________________。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.钢板镀锌可以防止锈蚀
B.羊毛、蚕丝、棉花的主要成分都是纤维素
C.高纯石英玻璃可用来制造光导纤维
D.生铁和普通钢都是铁碳合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,在金属元素与非金属元素的分界线附近可以找到( )
A.作为催化剂的材料
B.电子工业上的半导体材料
C.制造农药的材料
D.制造耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Sorbicillin (简称化合物X)是生产青霉素时的一个副产品,其结构简式如右下图所示。 下列有关化合物X的说法正确的是

A. 分子中所有碳原子可能处于同一平面
B. 1 mol化合物X可以与2 mol Na2CO3反应
C. 1mol化合物X可以与浓溴水发生取代反应消耗3molBr2
D. 化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com