
| A. | 在空气质量日报中CO2含量属于空气污染指数 | |
| B. | 日常生活中和医院常用无水乙醇杀菌消毒 | |
| C. | 绿色食品是指不含任何化学物质的食品 | |
| D. | 目前加碘食盐中主要添加的是KIO3 |
分析 A.二氧化碳不属于空气质量日报内容;
B.体积分数为75%的酒精溶液常用于灭菌消毒,此浓度杀菌力最强;
C.任何物质都由化学物质组成;
D.KIO3较为稳定,加碘食盐主要添加的是KIO3.
解答 解:A.目前计入空气污染指数的项目主要为:可吸入颗粒物、二氧化硫、二氧化氮,二氧化碳不属于空气质量日报内容,故A错误;
B.在75%的酒精作用下,乙醇能渗入细胞内,使蛋白质凝固变性,从而起到杀菌的作用,低于这个浓度,其渗透脱水作用减弱,杀菌力不强;而高于此浓度,则会使细菌表面蛋白质迅速脱水,凝固成膜,妨碍乙醇透入,削弱杀菌能力,对病毒无效,故B错误;
C.绿色食品是指在无污染的条件下种植、养殖、施有机肥料、不用高毒性、高残留农药、在标准环境、生产技术、卫生标准下加工生产、经权威机构认定并使用专门标志的安全、优质、营养类食品的统称,任何物质都由化学物质组成,故C错误;
D.KIO3较为稳定,为加碘食盐中添加剂,故D正确;
故选D.
点评 本题考查较为综合,为高考常见题型,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意常见物质的性质,牢固把握相关基础知识是解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 合成纤维和光导纤维都是新型有机非金属材料 | |
| B. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| C. | “玉不琢不成器”、“百炼方能成钢”发生的均为化学变化 | |
| D. | 造纸工艺中使用明矾,会导致纸张发生酸性腐蚀,使纸张变脆,易破损 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)已知在常温常压下:
(1)已知在常温常压下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 精铜板作阴极,纯铜片作阳极,CuSO4溶液作电解液 | |
| B. | 电解时,阴极发生氧化反应,则阴极发生的反应为:Cu2++2e-═Cu | |
| C. | 粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 | |
| D. | 电解铜的纯度可达99.95%~99.98% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 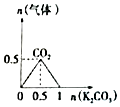 n (HCl)=1mol,K2CO3加入到HCl溶液中,在敝口容器中生成的气体 | |
| B. | 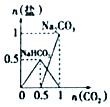 n(NaOH)=1mol,CO2通入到NaOH溶液中反应生成的盐 | |
| C. | 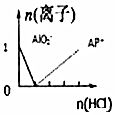 n(NaAlO2)=1mol,HCl加入到NaAlO2溶液中离子的存在情况 | |
| D. | 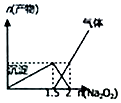 n(AlCl3)=1mol,Na2O2加入AlCl3溶液反应的产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
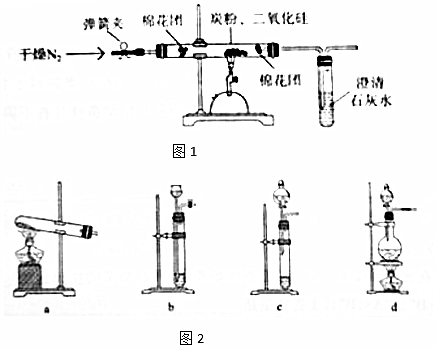
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
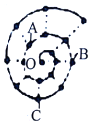 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中O点代表氢元素,下列说法中错误的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中O点代表氢元素,下列说法中错误的是( )| A. | O与A、B、C均能形成两种化合物 | |
| B. | A元素位于元素周期表ⅥA族 | |
| C. | B元素是图中金属性最强的元素 | |
| D. | B、C最高价氧化物的水化物可以相互反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com