
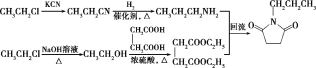
【题目】有机制药工业中常用以下方法合成一种药物中间体(G):
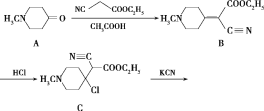

(1)G的分子式是___。
(2)化合物A中含氧官能团的名称为___。
(3)由C→D的反应类型为___;化合物E的结构简式为___。
(4)写出B→C的反应的化学方程式:___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应;
②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9;
③分子中含有氨基。
(6)已知:RCN![]() RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备
RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备![]() 的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH![]() CH2
CH2![]() CH2
CH2![]() CH3CH2Cl
CH3CH2Cl
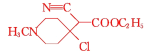
【答案】C11H18O2N2 羰基 取代反应 ![]()
![]() +HCl
+HCl![]()
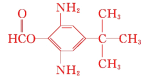 或
或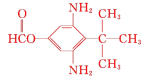
【解析】
⑴根据G的结构式数出G的分子式。
⑵化合物A中含氧官能团的名称为羰基。
⑶对比C、D的结构简式可知C→D反应类型,E与乙醇发生酯化反应得到F,由F的结构简式逆推得,E的结构简式。
⑷对比B、C的结构简式可知,B中碳碳双键与HCl发生加成反应生成C。
⑸根据同时满足条件的书写B的同分异构体。
⑹由F→G的转化可知,CH3CH2CH2NH2与CH3CH2OOCCH2CH2COOCH2CH3反应得到 ,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3。
,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3。
⑴根据G的结构式数出G的分子式是C11H18O2N2,故答案为:C11H18O2N2。
⑵化合物A中含氧官能团的名称为羰基,故答案为:羰基。
⑶对比C、D的结构简式可知,C中的—Cl被—CN取代生成D,所以C→D属于取代反应;由题图知,E与乙醇发生酯化反应得到F,由F的结构简式逆推得,E的结构简式为![]() ,故答案为:取代反应;
,故答案为:取代反应;![]() 。
。
⑷对比B、C的结构简式可知,B中碳碳双键与HCl发生加成反应生成C,B→C的反应的化学方程式为![]() +HCl
+HCl![]()
![]() ,故答案为:
,故答案为:![]() +HCl
+HCl![]()
![]() 。
。
⑸同时满足下列条件的B的同分异构体:①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应,说明含有甲酸与酚形成的酚酯基,即取代基为—OOCH,③分子中含有氨基,②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9,存在对称结构,还含有2个—NH2、1个—C(CH3span>)3,符合条件的B的同分异构体为 或
或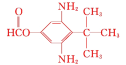 ,故答案为:
,故答案为: 或
或 。
。
⑹由F→G的转化可知,CH3CH2CH2NH2与CH3CH2OOCCH2CH2COOCH2CH3反应得到 ,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3,故答案为:
,CH3CH2Cl与KCN发生取代反应得到CH3CH2CN,用氢气还原得到CH3CH2CH2NH2,CH3CH2Cl在碱性条件下水解得到CH3CH2OH,然后与HOOCCH2CH2COOH反应得到CH3CH2OOCCH2CH2COOCH2CH3,故答案为:
 。
。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是
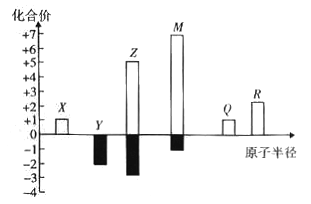
A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C9H12的苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是 ( )
A. 该有机物能发生加成反应,但不能发生取代反应
B. 该有机物不能使酸性高锰酸钾溶液和溴水褪色
C. 该有机物分子中的所有原子不可能在同一平面上
D. 该有机物的一溴代物最多有5种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①锌跟稀硫酸反应制H2,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,把氧化铝加入液态冰晶石中熔融后电解
⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
A.全部B.①③④⑤C.①②⑤D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A. I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B. II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据要求填空:
(1) 用系统命名法命名:______________;
用系统命名法命名:______________;
(2) 的分子式______________;
的分子式______________;
(3) ![]() 官能团的名称是________________。
官能团的名称是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄雪盐的工艺如下:
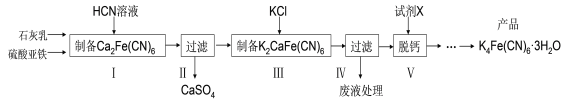
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为__________________________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为____________(填化学式)。
(3)步骤Ⅴ所用的试剂X是___________。(填化学式)
(4)工艺中用到剧毒的HCN溶液,含CN- 的废水必须处理后才能排放。
已知: HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
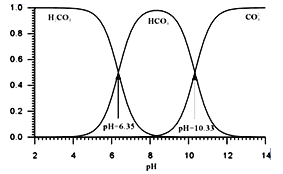
①NaCN的电子式为___________。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是_______,第二步反应的离子方程式为____________。
(5)已知蓝色染料普鲁士蓝的合成方法如下:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如下:
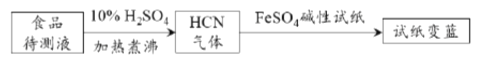
若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
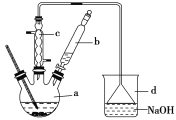
名称 | 苯 | 溴 | 溴苯 |
密度/(g·cm-3) | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置d的作用是___________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是___________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须用到的是________(填字母序号)。
a.重结晶b.过滤c.蒸馏d.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl, ②CH3OOH, ③Ba(OH)2,④Na2CO3,⑤KCl,⑥NH4Cl溶液pH由小到大的顺序为__________________(填写编号)。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=_________mol ·L-1(保留到小数点后一位)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈_________(填“酸性”,“中性”或“碱性”) ,请写出溶液中离子浓度间的一个等式:________________________________。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-) + c(CH3COOH)=______,m与n的大小关系是m_____n(填“ >”“=”或“<”)。
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7 ,则NH3·H2O的电离常数Ka=______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com