
| A. | 60 g SiO2晶体中含有Si-O键数目为2NA | |
| B. | 常温常压下,1.6 9 O2和O3的混合气体所含电子数为0.8NA | |
| C. | 1 mol/L AICl3溶液中,所含Al3+数目小于NA | |
| D. | 密闭容器中2 mol NO与l mol 02充分反应,产物的分子数为2NA |
分析 A、质量换算物质的量,1mol二氧化硅中含4mol硅氧键;
B、O2和O3均由氧原子构成;
C、溶液体积不明确;
D、NO2中存在平衡:2NO2?N2O4.
解答 解:A、60 g石英晶体屋子里的为1mol,结构中含有的Si-O键数目为4NA,故A错误;
B、O2和O3均由氧原子构成,故1.69g混合物中含有的氧原子的物质的量n=$\frac{1.69g}{16g/mol}$=0.1mol,而氧原子中含有8个电子,故0.1mol氧原子含有的0.8mol电子即0.8NA个,故B正确;
C、溶液体积不明确,故溶液中的铝离子的个数无法计算,故C错误;
D、2 mol NO与l mol 02生成2molNO2,但NO2中存在平衡:2NO2?N2O4,故生成的产物的分子小于2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定小于92.0 kJ | B. | 一定等于92.0 kJ | C. | 一定大于92.0 kJ | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
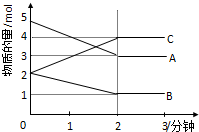 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| B. | 侯氏制碱法的工艺原理主要应用了物质熔沸点的差异 | |
| C. | 铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 | |
| D. | 用蘸有浓氨水的玻璃棒检验输送氯气的管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )
如图所示的电化学装置,可用于净化处理厕所排放废水中的尿素( H2 NCON H2),同时产生电能.下列有关说法不正确的是( )| A. | 右侧的多孔碳电极是原电池的负极 | |
| B. | 电解质溶液中H十向左侧移动 | |
| C. | 正极上发生还原反应:H2NCONH2+H2O-6e-═c-CO2+N2+6N+ | |
| D. | 电极上消耗标准状况下33.6LO2,电路中转移6 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A为O2,B为O3,它们质量相等时则容器中氧原子个数不相等 | |
| B. | 若A为NO2,B为N2O4,它们压强相等时则质量相等 | |
| C. | 若A为C2H4,B为C2H6,它们密度相等时则气体的物质的量相等 | |
| D. | 若A为CO2,B为C3H8,它们密度相等时则分子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com