
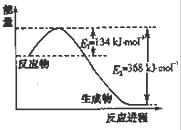
| t/�� | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
| 1 |
| 0.5 |
| 4��23 |
| 62 |
| 8 |
| 9 |


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ӵ����������в��÷���¯��Ŀ����Ϊ��ʹ��ǻ������ȼ�ճ�֣����ԭ�ϵ������� |
| B���ϳɰ����������в��ø��¸�ѹ��������Ϊ�����N2��H2��ת���� |
| C�����Ṥҵ�У��ڽӴ��Ұ�װ�Ƚ�������Ϊ��������ǻ������ȼ��ʱ�ų������� |
| D���������Ƽ�У�����ѭ����������CO2��NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͬϵ����ܻ�Ϊͬ���칹�� |
| B�����黯ѧ���ʱȽ��ȶ������ܱ��κ����������� |
| C�������������Ӧ��������CH3Cl��CH2Cl2��CHCl3����CCl4��������ȡ����Ӧ |
| D��C4H10�������ĸ�̼ԭ����һ��ֱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
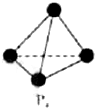 ����ѧ-ѡ��3�����ʽṹ�����ʡ�
����ѧ-ѡ��3�����ʽṹ�����ʡ�- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
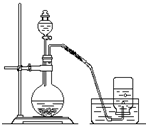 ������ͼ��ʾװ����ȡ������������ص�ʵ��̽����
������ͼ��ʾװ����ȡ������������ص�ʵ��̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
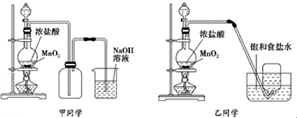
| ʵ����� | ʵ����� | ���� | ���� |
| �� | ��Ʒ����Һ | ��Һ��ɫ | ������ˮ��Ӧ�IJ�����Ư���� |
| �� | ����NaHCO3��ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ�����н�ǿ������ |
| ʵ����� | �� | �� |
| �� | ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com