
ˮ��һ����Ҫ����Ȼ��Դ���������������治��ȱ�ٵ����ʡ�ˮ�Ĵ�����Ҫ����ˮ�ľ�
������ˮ������Ӳˮ�����ͺ�ˮ�ĵ����ȡ�
(1)��ˮ�ĵ������õķ�����_________��
_________�����������ȡ�
(2)���������ǽ�������չ������һ�ֽϺ�
 �ĺ�ˮ������������ԭ����ͼ��ʾ��
�ĺ�ˮ������������ԭ����ͼ��ʾ��
�����������Ե缫���ĵ缫��ӦʽΪ __________________.
�ڵ�ˮ�ij���Ϊa��b��c�е�_________ ���ڡ�
��ij�����ų���Ũ��ˮ����Ԫ�صĺ���Ϊ0.68g/L���������������е�������
����Ϊ�嵥�ʣ�����l.Ox10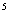 L��Ũ��ˮ�����µ����������Ϊ_________
L��Ũ��ˮ�����µ����������Ϊ_________ ��
��
(3) K2FeO4������ˮ�����õ�����������������ҵ�ϳ���Fe(NO3)3��Һ��ŨKCIO��Һ��ǿ���Ի���������K2FeO4���÷�Ӧ�����ӷ���ʽΪ___________________________.
(4)�ȼҵ����_________������������������ӽ���Ĥ���۵�⾫�Ƶı���ʳ��ˮ�� ��ʳ��ˮ�к�������MgCl2�������ӽ���Ĥ�����������ԭ����_______ (�����ӷ���ʽ��ʾ����
(5)��������ABS�ϳ�ʱ�������������ֵ��壺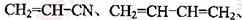 ��
��
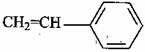 ����д��ABS�Ľṹ��ʽ_______________________________��
����д��ABS�Ľṹ��ʽ_______________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ں����������������Һ�У�����Fe(NO3)2�������Ȼ�ܹ������������������(����)
A��K����SO ��NH
��NH ��CO
��CO B��K����Ba2����OH����Cl��
B��K����Ba2����OH����Cl��
C��Na����H����Cl����S O
O D��Na����Mg2����Cl����
D��Na����Mg2����Cl���� NO
NO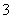
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ����������
A��ˮ�������c(H+)��c(OH-)=10-22����Һ��K+��Na����SO42����S2O32��
B����������Һ��Mg2����Cu2����Cl����SO42��
C��ʹ��̪���ɫ����Һ��NH4����K����AlO2����NO3��
D����0.1mol��L-1 KI����Һ��Fe3����Na����NO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1909��[b20] ��ѧ�ҹ�����ʵ�����״κϳ��˰���2007�껯ѧ�Ҹ���¡����ض��ڹ����о���֤ʵ�������뵪���ڹ������ϳɰ��ķ�Ӧ���̣�ʾ������ͼ��
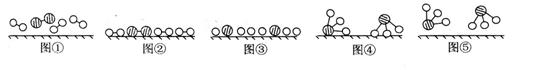
��1��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ���____��__��__�� ____��
��2����֪��4NH3(g) + 3O2(g) = 2N??2(g) + 6H2O(g); ��H= - 1266.8 kJ/mol
N2(g) + O2(g) = 2NO(g) ; ��H = + 180.5kJ/mol�� �����������Ȼ�ѧ����ʽΪ___�� _______��
��3��500���£���A��B���������о������ϳɰ��ķ�Ӧ�������̶�������������������ƶ���
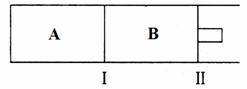
�ٵ��ϳɰ�������B�д�ƽ��ʱ��������к���1.0molN2��0.4molH2��0.4molNH3����ʱ�ݻ�Ϊ2.0L����������µ�ƽ�ⳣ��Ϊ_____�� _______�������¶Ⱥ�ѹǿ���䣬���������ͨ��0.36molN2��ƽ�⽫____�� ______������������������ƶ���
����A��B�������о�ͨ��xmolN2��ymolH2����ʼA��B�ݻ���ͬ���������¶Ȳ��䡣��Ҫƽ��ʱ����N2��A��B�������е����������ͬ����x��y֮���������Ĺ�ϵʽΪ__�� __��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�л���ķ���ʽΪC9H9ClO2 �������к���1��������������������ȡ������������NaHCO3��Һ��Ӧ��ͬ���칹�����ĿΪ���������������ͣ�
A��12�� B�� 15�� C��18�� D. 21��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���� �� ��
A��Li������ý�����F������÷ǽ���
B��Mg(OH)2���Ա�Ca(OH)2ǿ
C��Ԫ�����ڱ���7�����壬7�����壬1��0�壬1�����壬��16����
D��X2���ĺ��������ĿΪ10����X�ڵ�3���ڵڢ�A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ����ȡ����Ӧ����(����)
A��CH4��Cl2�Ļ��������պ���ɫ��dz
B����ϩͨ������KMnO4��Һ�У���Һ��ɫ
C��������ˮ��Ϻ���ˮ����ɫ
D����ϩͨ����ˮ�У���ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ݱ������������д���3He���ڣ����¹���3He��˵����ȷ���� �� ��
A�� ��4He��ͬ�������� B����4He��ͬλ��
C�� ��4He��һ������ D����4He��һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�⻯��ͭ(CuH)��һ�������ʣ���CuSO4��Һ����һ�֡���Ӧ���40��50 ��ʱ��Ӧ����������CuH���ȶ����ֽ⣻CuH����������ȼ�գ������ᷴӦ�ܲ������塣�����й��ƶ��д������ (����)
A������ġ���һ�ַ�Ӧ����л�ԭ��
B��CuH��������������ԭ��
C��CuH��Cl2===CuCl��HCl(ȼ��)
D��CuH��HCl===CuCl��H2��(����)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com