
| 29g/mol×(1+1)mol |
| 1mol |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
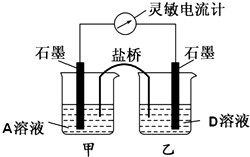 四种强电解质A、B、C、D的溶液,分别含有下列阴阳离子的各一种,且不重复.已知A溶液为黄色,含0.01mol的A溶液与含0.01mol的B溶液反应生成白色沉淀,再逐滴加入D溶液,白色沉淀最后转变为黄色沉淀.将C溶液滴在pH试纸的中部,显蓝色.
四种强电解质A、B、C、D的溶液,分别含有下列阴阳离子的各一种,且不重复.已知A溶液为黄色,含0.01mol的A溶液与含0.01mol的B溶液反应生成白色沉淀,再逐滴加入D溶液,白色沉淀最后转变为黄色沉淀.将C溶液滴在pH试纸的中部,显蓝色.| 阳离子 | K+、Fe3+、Ag+、Ca2+ |
| 阴离子 | Cl-、I-、CO32-、NO-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 |
| B、SO2溶于水,其水溶液能导电,说明SO2是电解质 |
| C、用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3) |
| D、某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀产生,说明溶液中有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一部分为Al(OH)3,一部分为Al3+ |
| B、全部为Al(OH)3 |
| C、一部分为Al(OH)3,一部分为AlO2- |
| D、全部为AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 盐酸浸泡 |
| 过滤 |
| 氧化处理 |
| 足量的 |
| NaOH溶液 |
| 过滤 |
| 洗涤 |
| 煅烧 |
| A、Al |
| B、Al(OH)3 |
| C、Al3+ |
| D、[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴加少量硫酸铜溶液 |
| B、增多铁片的用量 |
| C、改用98%的浓硫酸 |
| D、加入少量的CH3COONa固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com