
【题目】氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl2和NO在通常反应条件下制得,反应方程式为2NO(g)+Cl2(g) 2ClNO(g)。已知几种化学键的键能数据如表所示:

当Cl2与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为___kJ。(用数字和字母表示)
(2)温度一定时,在一个体积为1L的密闭容器中通入2moNO和1molCl2,10min时ClNO体积占气体总体积40%,反应开始到10min内NO的平均V(NO)=____mol·L-1·min-1。
(3)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,装置如图所示:
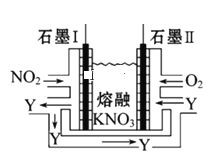
电池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ为电源___极,石墨Ⅱ附近发生的电极反应式为____。
【答案】(578-4a)kJ 0.1mol·L-1·min-1 正极 O2+2N2O5+4e-═4NO3-
【解析】
(1)2NO(g)+Cl2(g)![]() 2ClNO(g),反应的焓变△H=反应物总键能-生成物总键能,据此计算;
2ClNO(g),反应的焓变△H=反应物总键能-生成物总键能,据此计算;
(2)根据v=△C/△t计算;
(3)甲池工作时,NO2转变成N2O5,说明氮元素的化合价升高,石墨Ⅰ为负极,电极反应式为NO2+NO3--e-=N2O5,石墨Ⅱ为正极O2+2N2O5+4e-═4NO3-。
(1)2NO(g)+Cl2(g)![]() 2ClNO(g),1mol Cl2参与反应发生焓变△H=243KJ·mol-1+2×630KJ·mol-1-2×(aKJ·mol-1+607KJ·mol-1)=(289-2a)kJ·mol-1,此时转移2mol电子,则有4mol电子转移时,热量变化为(578-4a)kJ;
2ClNO(g),1mol Cl2参与反应发生焓变△H=243KJ·mol-1+2×630KJ·mol-1-2×(aKJ·mol-1+607KJ·mol-1)=(289-2a)kJ·mol-1,此时转移2mol电子,则有4mol电子转移时,热量变化为(578-4a)kJ;
(2)反应后各物质变化为
2NO+Cl2=2ClNO
起始物质的量 2 1 0
转化物质的量 2x x 2x
平衡物质的量 2-2x 1-x 2x
2x/(2-2x+1-x+2x)=0.4
x=0.5
V(NO)=![]() 0.1mol·L-1·min-1。
0.1mol·L-1·min-1。
(3)甲池工作时,NO2转变成N2O5,说明氮元素的化合价升高,石墨Ⅰ为负极,电极反应式为NO2+NO3--e-=N2O5,石墨Ⅱ为正极,电极反应:O2+2N2O5+4e-═4NO3-。


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH2=-565kJ·mol-1
(1)在一定条件下N2和O2会转化为NO,写出该反应的热化学方程式:_________。
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4mol CO,在催化剂存在的条件下发生反应,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后n(CO)=________mol,关于该平衡的下列说法正确的是________。
a.增大压强,平衡一定向右移动
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
d.达到平衡后v正(NO)=2v逆(N2)
(3)其他条件相同,t min时不同温度下测得NO的转化率如图所示。

A点的反应速度v正________(填“>”、“<”或“=”)v逆,A、B两点反应的平衡常数较大的是________(填“A”或“B”)。
(4)已知HNO2的电离常数Ka=7.1×10-4mol·L-1;
NH3·H2O的电离常数Kb=1.7×10-5mol·L-1
则0.1mol·L-1NH4NO2溶液中离子浓度由大到小的顺序是____________________________,
常温下NO2-水解反应的平衡常数Kh=________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是

A. 反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 图中X点所示条件下,延长反应时间能提高NO转化率
C. 图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是日常生活中的常用调味品。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。
(2)由A分别和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示)。
(3)A、B、E形成的离子化合物电子式为____________,其中存在的化学键类型为____________。
(4)D最高价氧化物的水化物的化学式为________________。
(5)单质D在充足的单质E中燃烧,反应的化学方程式为__________________;D在不充足的E中燃烧,生成的主要产物的化学式为__________。
(6)单质E与水反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X(仅含三种短周期元素)是一种络合氢化物的储氢材料,在400℃下分解,放出氢气。X中某种元素的单质常用来制造信号弹和烟火,某研究小组为了探究A的组成和性质,设计并完成了如下实验。(金属互化物--全部由金属元素组成的化合物)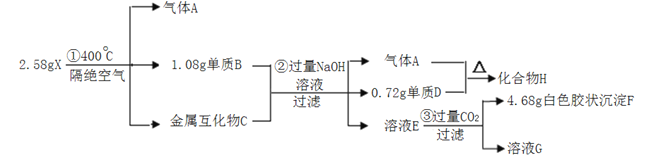
(1)写出单质D对应的阳离子结构示意图:_____。
(2)X在400℃下分解的化学方程式:_____。
(3)写出单质B与NaOH溶液反应的离子方程式:____。
(4)化合物H___(填“可能”或“不可能”)与水发生反应产生H2,判断理由_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,现有如下图中物质的转化关系,

试回答:(1)写出B的化学式________D的化学式_________,G俗称___________
(2)写出④的化学方程式_________________________________________
(3)写出⑥的离子方程式__________________写出⑦的离子方程式_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2 是中学化学中的常见气体,也是大气污染物的主要组成成分。回答下列问题:

⑴甲组同学利用下列装置制备并收集干燥的 SO2:

装置Ⅰ中盛装亚硫酸钠的仪器名称是_______,装置 II 的作用是对 SO2 气体进行干燥,该装置中所盛 试剂名称为_________,装置 III 为集气装置,应选取填入 III 中的集气装置为___________(选填字母代号)。
⑵乙组同学利用下列装置制备 SO2 并探究其性质:

①该组同学的实验装置中,依次连接的合理顺序为a→_________。装置C中饱和NaHSO3溶液的作用是________。
②能证明SO2具有还原性的现象是___________,该反应的离子方程式为_________________。
③装置B的作用吸收SO2尾气,该装置中盛装的试剂是_______________。
⑶设计实验证明H2SO3为弱电解质:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某港口化学品堆场发生火灾,消防队在未被告知着火可燃物类别的情况下,用水灭火时,发生了剧烈爆炸。事后有关部门初步认定危化品部分清单:钾、钠、氯酸钾、烧碱、氯化铵。试回答:
⑴请你分析用水灭火时,随后发生了剧烈爆炸的原因是_____________________________。
⑵请写出氯化铵中NH4+的检验方法____________________________(简要说明操作步骤)。
⑶钠燃烧产物中可作为消防员呼吸面具供氧剂的是_________________(写化学式)。
⑷硝酸钾受热分解产生KNO2和O2,写出该反应的化学方程式______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com