
磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是_________________________________________________________。
(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:
Cr2O +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
①在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、________和________。
②若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________mol·L-1。
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________(填序号)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4·2H2O。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为________。
答案 (1)加快铁与稀硫酸反应速率
(2)①用蒸馏水洗净 用K2Cr2O7标准溶液润洗2~3次 ② ③AB
③AB
(3)Fe(OH)3(或氢氧化铁)
解析 (1)温度越高反应速率越快,因此加热可以加快反应的速率。
(2)①滴定管要先用蒸馏水洗涤,再用待装液体润洗。②根据题给离子方程式可知,n(Fe2+)=6n(Cr2O ),c(Fe2+)=
),c(Fe2+)=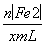 =
=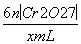 =
= mol·L-1。③加入过量的H2O2,可以使Fe2+充分被氧化;缓慢滴加H2O2并搅拌,可以使反应更充分;加热会使H2O2发生分解;加入氨水会使Fe2+转化为沉淀。故答案为AB。
mol·L-1。③加入过量的H2O2,可以使Fe2+充分被氧化;缓慢滴加H2O2并搅拌,可以使反应更充分;加热会使H2O2发生分解;加入氨水会使Fe2+转化为沉淀。故答案为AB。
(3)因为碱性溶液中Fe3+反应生成红褐色的Fe(OH)3沉淀,从而使得到的FePO4·2H2O固体呈棕黄色。


科目:高中化学 来源: 题型:
Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:

(1)A、B、C三者的关系是____________。
(2)A的分子式为__________,C的名称为__________。
(3)写出C的同分异构体的结构简式:_______________________________________。
Ⅱ.下图均能表示甲烷的分子结构,其中更能反映其真实的存在状况的是__________(填字母)。


查看答案和解析>>
科目:高中化学 来源: 题型:
下面是小王在医院做的血常规检查报告单的部分内容,小王应该注意补充的微量元素是( )
| No | 项目 | 结果 | 正常范围参考值 | 单位 |
| 1 | 红细胞计数 | 2.3 | 3.5~5 | 1×1012/L |
| 2 | 血红蛋白 | 75 | 110~150 | g/L |
| 3 | 血小板计数 | 205.5 | 100~300 | 109/L |
A.硒 B.锌 C.铁 D.碘
查看答案和解析>>
科目:高中化学 来源: 题型:
 请将左栏中物质的特性于右栏中物质的用途连接起来.
请将左栏中物质的特性于右栏中物质的用途连接起来.
 特性 用途
特性 用途
 银有良好的导电性,不易氧化 淡化海水
银有良好的导电性,不易氧化 淡化海水
 玻璃钢质轻、坚硬、不导电 高档电器插头
玻璃钢质轻、坚硬、不导电 高档电器插头
 麦秆、稻草易被微生物分解 制造印刷电路板
麦秆、稻草易被微生物分解 制造印刷电路板
 高分子膜能选择性通过某些物质 制造环保饭盒
高分子膜能选择性通过某些物质 制造环保饭盒
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化尿素是一种无毒无味的白色粉末,是一种新型的漂白剂与消毒剂。它的合成原理:CO(NH2)2+H2O2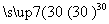 CO(NH2)2·H2O2。
CO(NH2)2·H2O2。
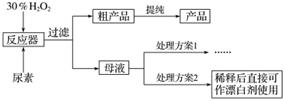
请回答下列问题:
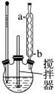
(1)流程图中反应器的装置如图所示,推测该反应的加热方式是______________________;回流管中冷水流从____________口流入;搅拌器选用的材质是玻璃而不是铁质或铝质材料的原因是__________________________。
(2)母液处理方案1可以是______________(用文字表达)。若欲从母液中分离出H2O2和尿素,可采用的操作是______(选填序号)。
A.盐析、过滤 B.减压蒸馏、结晶
C.分液、过滤 D.常压蒸馏、萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品2.000 g,溶解,在250 mL容量瓶中定容。准确量取25.00 mL于锥形瓶中,加入1 mL 6 mol·L-1的硫酸,然后用0.100 0 mol·L-1 KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液8.00 mL(KMnO4溶液与尿素不反应)。
①完成并配平方程式:______MnO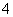 +______H2O2+________________________
+______H2O2+________________________
H+===______Mn2++______H2O+______。
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量________。(填“偏高”、“偏低”或“不变”)
③根据滴定结果,可确定产品中活性氧的质量分数为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在密闭容器中将物质的量相同的下列各组气体混合,完全反应后容器中压强没有发生变化的是 ( )
A.H2S和SO2 B.NO和O2 C.HI和Cl2 D.H2S和Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
把Al和Fe3O4粉配成铝热剂,分成两等份,前一份在高温下恰好完全反应,然后将生成物与足量的盐酸充分反应,后一份直接加入足量的氢氧化钠溶液使之充分反应,前后两种情况下生成气体的物质的量之比为 ( )
A.1︰3 B.9︰8 C.3︰4 D.4︰3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒沙特列原理来解释的是( )
A.Fe(SCN)3溶液中加入固体KSCN后颜色变深
B.密闭容器中发生反应H2+I2=2HI,增大压强时,容器中颜色加深。
C.将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应
D.用过量空气煅烧硫铁矿可以提高硫铁矿的利用率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com