
| CH3COOH | HCN | H2CO3 |
| K=1.75”Į10-5 | K=4.9”Į10-10 | Ki1=4.3”Į10-7 Ki2=5.6”Į10-11 |
| A£® | ĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2µÄĄė×Ó·½³ĢŹ½£ŗCN-+H2O+CO2ØTHCN+HCO3- | |
| B£® | 25”ꏱ£¬·“Ó¦CH3COOH+CN-?HCN+CH3COO-µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ3.57”Į104 | |
| C£® | ÖŠŗĶµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COOHŗĶHCNČÜŅŗ£¬ĻūŗÄNaOHµÄĮæĒ°Õߊ”ÓŚŗóÕß | |
| D£® | µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COONaŗĶNaCN»ģŗĻČÜŅŗÖŠ£ŗc£ØCH3COO-£©£¾c£ØCN-£©£¾c£ØOH-£©£¾c£ØH+£© |
·ÖĪö A£®ĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2£¬ÓÉÓŚĖįŠŌ£ŗH2CO3£¾HCN£¾HCO3-£¬¹Ź·“Ӧɜ³ÉHCNŗĶĢ¼ĖįĒāÄĘ£¬²»ÄÜÉś³É¶žŃõ»ÆĢ¼£¬¹Ź·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖNaCN+H2O+CO2=HCN+NaHCO3£»
B£®·“Ó¦CH3COOH+CN-?HCN+CH3COO-µÄ»ÆŃ§Ę½ŗā³£ŹżK=$\frac{c£ØHCN£©c£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©c£ØC{N}^{-}£©}$=$\frac{c£ØHCN£©c£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©c£ØC{N}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{K£ØC{H}_{3}COOH£©}{K£ØHCN£©}$£»
C£®ÖŠŗĶµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COOHŗĶHCNČÜŅŗ£¬Ē”ŗĆĶźČ«·“Ó¦ŠčŅŖĒāŃõ»ÆÄĘĪļÖŹµÄĮæĻąĶ¬£»
D£®ĖįŠŌCH3COOH£¾HCN£¬µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COONaŗĶNaCN»ģŗĻČÜŅŗÖŠ£¬CN-Ąė×ÓĖ®½ā³Ģ¶Č“óÓŚCH3COO-£®
½ā“š ½ā£ŗA£®ĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2£¬ÓÉÓŚĖįŠŌ£ŗH2CO3£¾HCN£¾HCO3-£¬¹Ź·“Ӧɜ³ÉHCNŗĶĢ¼ĖįĒāÄĘ£¬²»ÄÜÉś³É¶žŃõ»ÆĢ¼£¬¹Ź·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCN-+H2O+CO2ØTHCN+HCO3-£¬¹ŹAÕżČ·
B£®·“Ó¦CH3COOH+CN-?HCN+CH3COO-µÄ»ÆŃ§Ę½ŗā³£ŹżK=$\frac{c£ØHCN£©c£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©c£ØC{N}^{-}£©}$=$\frac{c£ØHCN£©c£ØC{H}_{3}CO{O}^{-}£©}{c£ØC{H}_{3}COOH£©c£ØC{N}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{K£ØC{H}_{3}COOH£©}{K£ØHCN£©}$=$\frac{1.75”Į1{0}^{-5}}{4.9”Į1{0}^{-10}}$=3.57”Į104£¬¹ŹBÕżČ·£»
C£®ÖŠŗĶµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COOHŗĶHCNČÜŅŗ£¬¶¼ŹĒŅ»ŌŖĖįĻūŗÄNaOHµÄĮæĻąĶ¬£¬¹ŹC“ķĪó£»
D£®ĖįŠŌCH3COOH£¾HCN£¬µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COONaŗĶNaCN»ģŗĻČÜŅŗÖŠ£¬CN-Ąė×ÓĖ®½ā³Ģ¶Č“óÓŚCH3COO-£¬c£ØCH3COO-£©£¾c£ØCN-£©£¾c£ØOH-£©£¾c£ØH+£©£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµēĄėĘ½ŗā”¢µēĄėĘ½ŗā³£ŹżµÄ¼ĘĖć”¢ŃĪĄąĖ®½āÓ¦ÓĆ£¬ĖįŌ½Čõ¶ŌÓ¦ŃĪĖ®½ā³Ģ¶ČŌ½“ó£¬ĢāÄæÄѶČÖŠµČ£®


 ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø
ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 2Z£Øg£©·“Ó¦ĆæĻūŗÄ1molY·Å³öakJµÄČČĮ棬ĻÖÓŠ¼×”¢ŅŅĮ½ČŻ»żĻąµČĒŅ¹Ģ¶ØµÄĆܱÕČŻĘ÷£¬ŌŚ±£³ÖøĆĪĀ¶Čŗć¶ØµÄĢõ¼žĻĀ£¬ĻņĆܱÕČŻĘ÷¼×ÖŠĶØČė2molXŗĶ1molY£¬“ļµ½Ę½ŗāדĢ¬Ź±£¬·Å³öČČĮæbkJ£»ĻņĆܱÕČŻĘ÷ŅŅÖŠĶØČė1molXŗĶ0.5molY£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæckJ£¬ĒŅ£¬Ōņa”¢b”¢cµÄÖµ»ņ¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©
2Z£Øg£©·“Ó¦ĆæĻūŗÄ1molY·Å³öakJµÄČČĮ棬ĻÖÓŠ¼×”¢ŅŅĮ½ČŻ»żĻąµČĒŅ¹Ģ¶ØµÄĆܱÕČŻĘ÷£¬ŌŚ±£³ÖøĆĪĀ¶Čŗć¶ØµÄĢõ¼žĻĀ£¬ĻņĆܱÕČŻĘ÷¼×ÖŠĶØČė2molXŗĶ1molY£¬“ļµ½Ę½ŗāדĢ¬Ź±£¬·Å³öČČĮæbkJ£»ĻņĆܱÕČŻĘ÷ŅŅÖŠĶØČė1molXŗĶ0.5molY£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæckJ£¬ĒŅ£¬Ōņa”¢b”¢cµÄÖµ»ņ¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©| A£® | 2b=c | B£® | a=b | C£® | a£¾2c | D£® | ŅŌÉĻ¶¼²»ÕżČ· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 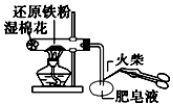 ŃéĢś·ŪÓėĖ®ÕōĘų·“Ó¦²śÉśµÄĒāĘų | |
| B£® |  ·ÖĄėĮ½ÖÖ»„Čܵ«·ŠµćĻą²ī½Ļ“óµÄŅŗĢå»ģŗĻĪļ | |
| C£® |  ŅŅĖįŅŅõ„µÄÖʱøŃŻŹ¾ŹµŃé | |
| D£® |  Ģ¼ĖįĒāÄĘŹÜČČ·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ĻÖĻó | ½įĀŪ»ņ½āŹĶ |
| A | ½«Ļ”ŃĪĖįµĪČė¼ÓÓŠ·ÓĢŖµÄNa2SiO3ČÜŅŗÖŠ£¬±ß¼Ó±ßÕšµ“£¬ | ŗģÉ«±äĒ³²¢½Ó½üĻūŹ§ | ÓŠ¹čĖį½ŗĢåÉś³É |
| B | ĀČ»ÆÄĘ¾§Ģåµ¼µēŹµŃé | ²»µ¼µē | ¾§Ģå²»“ęŌŚĄė×Ó |
| C | AgIŠü×ĒŅŗÖŠµĪČėNa2SČÜŅŗ | ¹ĢĢå±äŗŚ | Ksp£ØAg2S£©£¾Ksp£ØAgI£© |
| D | ²āĮæH2CO3µÄµēĄė³£Źż | Ka1£¾ka2 | H2CO3Ņ»¼¶µēĄė³£Źż²śÉśµÄH+¶Ō¶ž¼¶µēĄėĘšŅÖÖĘ×÷ÓĆ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ČēĶ¼1£¬ĻņČŻĮæĘæÖŠ×ŖŅĘČÜŅŗ | |
| B£® | Ķ¼2£¬ÓƱź×¼ÅØ¶ČµÄNaOHČÜŅŗµĪ¶ØĪ“ÖŖÅØ¶ČµÄŃĪĖį | |
| C£® | Ķ¼3£¬ŹµŃéŹŅÓĆÅØĮņĖįŗĶŅŅ“¼¹²ČČÖĘŅŅĻ© | |
| D£® | Ķ¼4£¬ŃéÖ¤H2ŌŚCl2ÖŠČ¼ÉÕµÄŹµŃéĻÖĻó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ¼×Ķ¼ĪŖŅ»ÖÖŠĀŠĶĪŪĖ®“¦Ąķ×°ÖĆ£¬øĆ×°ÖĆæÉĄūÓĆŅ»ÖÖĪ¢ÉśĪļ½«ÓŠ»ś·ĻĖ®µÄ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄÜ£®ŅŅĶ¼ŹĒŅ»ÖÖ¼ŅÓĆ»·±£ŠĶĻū¶¾Ņŗ·¢ÉśĘ÷£¬ÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®£®ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø””””£©
¼×Ķ¼ĪŖŅ»ÖÖŠĀŠĶĪŪĖ®“¦Ąķ×°ÖĆ£¬øĆ×°ÖĆæÉĄūÓĆŅ»ÖÖĪ¢ÉśĪļ½«ÓŠ»ś·ĻĖ®µÄ»ÆѧÄÜÖ±½Ó×Ŗ»ÆĪŖµēÄÜ£®ŅŅĶ¼ŹĒŅ»ÖÖ¼ŅÓĆ»·±£ŠĶĻū¶¾Ņŗ·¢ÉśĘ÷£¬ÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®£®ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Nµē¼«ÉĻĆæĻūŗÄ22.4LĘųĢå£Ø±ź×¼×“æö£©Ź±£¬ŌņÓŠ4molH+ĶعżÖŹ×Ó½»»»Ä¤“Óøŗ¼«ĒųŅĘĻņÕż¼«Ēų | |
| B£® | Čō×°ÖĆŅŅĖłŠčµÄµēÄÜĄ“×Ō×°ÖĆ¼×£¬Ōņb¼«Ó¦ÓėX ¼«Į¬½Ó | |
| C£® | ČōÓŠ»ś·ĻĖ®ÖŠÖ÷ŅŖŗ¬ÓŠĘĻĢŃĢĒ£¬Ōņ×°ÖĆ¼×ÖŠM¼«·¢ÉśµÄµē¼«Ó¦ĪŖC6H12O6+6H2O-24e-=6CO2”ü+24H+ | |
| D£® | ÓÉ×°ÖĆŅŅÖĘµĆµÄ¼ŅÓĆĻū¶¾ŅŗµÄÖ÷ŅŖ³É·ÖŹĒNaClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņFeI2ČÜŅŗÖŠµĪ¼ÓÉŁĮæĀČĖ®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe2++Cl2ØT2Fe3++2Cl- | |
| B£® | ÄÜŹ¹pHŹŌÖ½ĻŌÉīŗģÉ«µÄČÜŅŗÖŠ£¬Fe3+”¢Cl-”¢Ba2+”¢Br-£¬Äܹ»“óĮæ¹²“ę | |
| C£® | ĻņNaClOČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĢ¼µÄĄė×Ó·½³ĢŹ½£ŗ2ClO-+CO2+H2OØT2HClO+CO32- | |
| D£® | ĻņäåĖ®ÖŠ¼ÓČė×ćĮæĀČ»ÆŃĒĢśČÜŅŗÄÜŹ¹äåĖ®±ä³ÉĪŽÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶“󊔣ŗM£¼N£¼Q£¼R | |
| B£® | WÖŠµÄŅõŃōĄė×ÓøöŹż±ČĪŖ1£ŗ1£¬ŹōÓŚĄė×Ó»ÆŗĻĪļ | |
| C£® | QµÄijµ„ÖŹæÉ×÷Ė®µÄĻū¶¾¼Į£¬øƵ„ÖŹŌŚ“óĘųÖŠŗ¬ĮæŌ½¶ą£¬¶ŌČĖĢåŌ½ÓŠŅę | |
| D£® | MŗĶN”¢Q¾łÄÜŠĪ³É¼Čŗ¬¼«ŠŌ¼üÓÖŗ¬·Ē¼«ŠŌ¼üµÄ·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{b-a}{2a-b}$ | B£® | $\frac{a-b}{2b-a}$ | C£® | $\frac{2a-b}{b-a}$ | D£® | $\frac{2a+b}{b+a}$ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com