
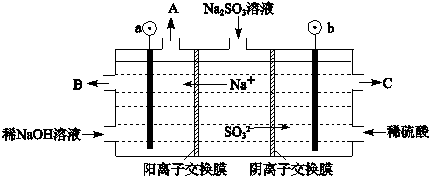
| 0.5mol |
| 2L?5min |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� | ��Ⱦָ�� | ��Ҫ��Ⱦ�� | ������������ | ��������״�� |
| �� | 55 | SO2 | II | �� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�013
��ҵ����������β���ų��ĵ���������ǿ�������Ҫ��ȾԴ��Ϊ������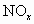 ����Ⱦ����ͨ������������
����Ⱦ����ͨ������������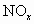 ��ԭΪ������
��ԭΪ������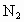 ��
��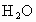 ������
������
����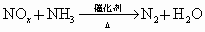
�������к���������NO��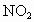 �Ļ������3.0L����ͬ��ͬѹ�µ�3.5L
�Ļ������3.0L����ͬ��ͬѹ�µ�3.5L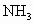 ǡ��ʹ�û��������ȫ��Ӧת��Ϊ
ǡ��ʹ�û��������ȫ��Ӧת��Ϊ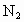 ����������NO��
����������NO��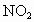 ���������
���������
[����]
|
A��1:4 |
B��1:3 |
|
C��1:2 |
D��1:1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�긣������ܼ����ѧ�߶���ѧ�����п����Ŀƻ�ѧ�Ծ����������� ���ͣ�ʵ����
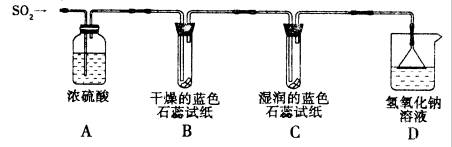
��12�֣��±��Ǽ׳���ij�տ����������棺
| ���� | ��Ⱦָ�� | ��Ҫ��Ⱦ�� | ������������ | ��������״�� |
| �� | 55 | SO2 | II | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ̩���н�����������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�о���������������ȴ�����Ⱦ�������������Ҫ���塣
��1��úȼ�ղ����������к��У�SO2��CO2��PM2.5�ȣ���������ֱ���ŷŵ������У���������Ҫ���������� ������д��ĸ��ţ�
A������ЧӦ B������ C���۳���Ⱦ D��ˮ�帻Ӫ����
������SO2�ķ���ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ��������ڷ�������Ĺ����У����õ�ʯ��ʯ��Һ�ڽ�������װ��ǰ����ͨһ��ʱ��Ķ�����̼��������������Ч�ʣ�����ʱ���ƽ�Һ��pHֵ����ʱ��Һ���е���������ƿ��Ա���������������������ơ�
������̼��ʯ��ʯ��Һ��Ӧ�õ��IJ���Ϊ ��
��������Ʊ���������������������ƵĻ�ѧ����ʽΪ ��
��2�����������һ�������ȼҵ��Ʒ������������������ķ����������������£�
 ��ҵ�����У�����۵ķ�Ӧ����Ϊ
��
��ҵ�����У�����۵ķ�Ӧ����Ϊ
��
�ù���������D������Ϊԭ��ѭ�����ã����Ļ�ѧʽΪ ��
д������ڷ�Ӧ�����ӷ���ʽ ��
��3������β���к��еĵ������NOx�����γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ ����β���п�������ʱ��NOX�ڴ�ת�����б���ԭ��N2�ų���д��NO��CO��ԭ�Ļ�ѧ����ʽ_ ��
��4����ҵ�ϳ���Na2CO3��Һ�������������
��֪��NO������Na2CO3��Һ��Ӧ
NO + NO2 + Na2CO3 = 2NaNO2 + CO2
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2
����������Na2CO3��Һ��ȫ����NO��NO2�Ļ������8.96L�����������NO��NO2�������Ϊ1��3�������չ����в��������ڱ�״���µ����Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com