
已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。
试回答下列有关的问题:
(1)写出F元素的电子排布式________。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为________。
(3)已知C、E两种元素合成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是________。
(4)B、C、D、E的第一电离能由大到小的顺序是________(写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______________(写化学式)。
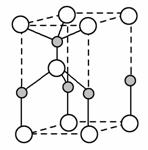
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:
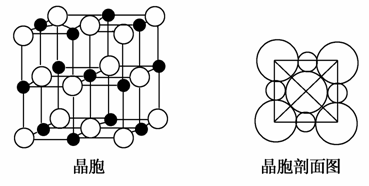
晶胞中距离一个B+最近的B+有________个。
若晶体密度为ρg·cm-3,阿伏加德罗常的值用NA表示,则E-的离子半径为________cm(用含NA与ρ的式子表达)。
解析 A、B、C、D、E、F六种元素,原子序数依次增大,由“A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等”推出A为O,由“B是短周期中原子半径最大的元素”推出B为Na,由“C元素3p能级半充满”推出C为P,由“F是第四周期未成对电子最多的元素”推出F为Cr,由“E是所在周期电负性最大的元素”及原子序数大小关系推出E为Cl,则D为S。(2)含四个原子的A的氢化物为H2O2,其氧原子的杂化轨道类型为sp3。(3)CE3和CE5为PCl3和PCl5,PCl3是极性分子,空间构型为三角锥形,PCl5为非极性分子。(4)同周期主族元素第一电离能从左到右有增大的趋势,但第ⅤA族反常,第一电离能由大到小的顺序是Cl>P>S>Na。四种元素最高价氧化物对应的水化物分别是NaOH、H3PO4、H2SO4、HClO4,NaOH是碱,H3PO4是中强酸,H2SO4、HClO4都是强酸,物质的量浓度相同时,pH由大到小顺序为NaOH>H3PO4>HClO4>H2SO4。(5)与Na+最近的Na+共有12个。设正方形(晶胞剖面图)的边长为a cm、Cl-的半径为r cm,ρa3=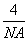 ×58.5,得a=
×58.5,得a=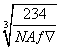 ,r=
,r=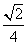 a=
a=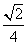
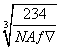 。
。
答案 (1)1s22s22p63s23p63d54s1或3d54s1
(2)sp3
(3)三角锥形
(4)Cl>P>S>Na NaOH>H3PO4>HClO4>H2SO4
(5)12 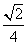
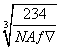


科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O3•5H2O
反应原理:Na2SO3(aq)+S(s)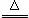 Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。
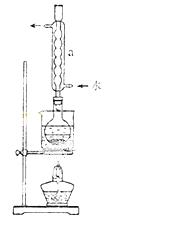
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的名称是 ,其作用是 。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。
反应原理为:2S2O32‾+I2=S4O62-+2I‾
(5)滴定至终点时,溶液颜色的变化: 。
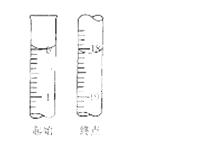
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。产品的纯度为(设Na2S2O3•5H2O相对分子质量为M) 。
III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol金属Al全部转化为Al(OH)3,消耗HCl a mol,NaOH b mol,则a+b的最小值为( )
A.4 B.6 C.8 D.16
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个氮原子的氮气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数小于3NA
C.在常温常压下,11.2L Cl2含有的分子数为0.5NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
卤族元素包括F、Cl、Br等。
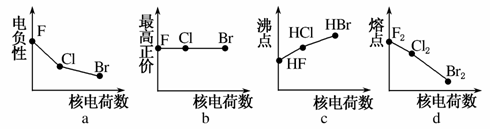
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是________。
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,右图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为________,该功能陶瓷的化学式为________。
(3)BCl3和NCl3中心原子的杂化方式分别为________和________。第一电离能价于B、N之间的第二周期元素有________种。
(4)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对电子的原子是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A(g)+3B(g)  2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
A. v(A)=0.01 mol/(L•s) B. v(B)=0.04 mol/(L•s)
C.v(B)=0.60mol/(L•min) D. v(C)=1.0mol/(L•min)
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )
| 实验 | 反应 温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
浓度为2 mol/L的NaOH溶液的正确含义是( )
A.在2 L水中溶有80克的NaOH
B.80克NaOH溶于1 L水配成的溶液
C.在1升溶液中含有80克NaOH
D.在2 L溶液中含有80克NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com