
今年1月12日,我国3名潜水员圆满完成首次300米饱和潜水作业,实现“下五洋捉鳖”的壮举.
①潜水员乘坐的潜水钟以钢铁为主要制造材料.钢铁容易在潮湿空气中发生电化学腐蚀,其负极的电极反应式是 , .
②潜水员需要均衡的膳食结构.糖类、油脂、蛋白质都能为人体提供能量.某品牌高钙梳打的配料标签如右图所示.在所列配料中,富含糖类的是 ,植物油在体内水解最终产物是高级脂肪酸和 .碳酸氢钠、碳酸钙可调节人体内的过多的胃酸,写出碳酸钙与胃酸反应的离子方程式为 .
③运载潜水钟的母船会产生大量废水和垃圾.科学实验的含汞离子废水 需要处理后再排放,可加入适量的硫化钠溶液,使汞离子变成 (填化学式)沉淀而除去.

| 营养均衡与人体健康的关系;金属的电化学腐蚀与防护. | |
| 分析: | ①钢铁容易在潮湿空气中发生电化学腐蚀,Fe作负极,失去电子发生氧化反应; ②小麦粉中富含淀粉,油脂在人体中水解最终产物是高级脂肪酸和甘油,胃酸的主要成分是盐酸,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水; ③硫化汞是沉淀,难溶于水,因此废水中的汞离子与硫化钠溶液中的硫离子反应生成HgS沉淀. |
| 解答: | 解:①钢铁容易在潮湿空气中发生电化学腐蚀,Fe作负极,失去电子发生氧化反应,其负极的电极反应式是Fe﹣2e﹣=Fe2+, 故答案为:Fe﹣2e﹣=Fe2+; ②小麦粉中富含淀粉,淀粉属于糖类,植物油属于油脂,油脂在人体中水解最终产物是高级脂肪酸和甘油,胃酸的主要成分是盐酸,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O, 故答案为:小麦粉;甘油;CaCO3+2H+=Ca2++CO2↑+H2O; ③③硫化汞是沉淀,难溶于水,因此废水中的汞离子与硫化钠溶液中的硫离子反应生成HgS沉淀, 故答案为:HgS. |
| 点评: | 本题考查了电极反应式书写及物质的性质,难度不大,掌握钢铁的电化学腐蚀原理和物质的性质是解题的关键,注意化学与生活的联系. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列物质属于同系物的是( )
|
| A. | CH3CH2CH2OH与CH3CH2CH2CH2OH |
|
| B. | ﹣OH与CH3CH2CHO |
|
| C. | CH3COOH与HCOOCH3 |
|
| D. | CH2ClCH2CH2Cl与CH3CH2CH2CH2Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是几种常见的化学电源示意图,有关说法不正确的是 ( )
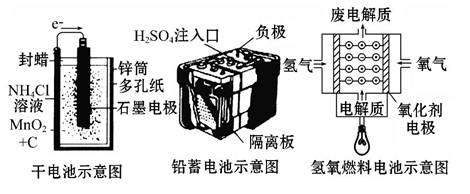
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍.下列说法正确的是( )
|
| A. | R的原子半径比Z的大 |
|
| B. | R的氢化物的热稳定性比W的强 |
|
| C. | X与Y形成的化合物只有一种 |
|
| D. | Y的最高价氧化物的水化物的酸性比W的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:
Ni2+(高浓度)>H+>Ni2+(低浓度)
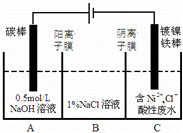
|
| A. | 碳棒上发生的电极反应:4OH﹣﹣4e﹣═O2↑+2H2O |
|
| B. | 电解过程中,B中NaCl溶液的物质的量浓度将不断减少 |
|
| C. | 为了提高Ni的产率,电解过程中需要控制废水pH |
|
| D. | 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求回答下列问题:
(1)①反应Cl2+H2O⇌H++Clˉ+HClO其化学平衡常数K的表达式为:
②在25℃下,将a mol•L﹣1的氨水与0.01mol•L﹣1的盐酸等体积混合,反应平衡时溶液中c(NH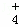 )=c(Cl﹣),试用含a的代数式表示NH3•H2O的电离常数Kb= .
)=c(Cl﹣),试用含a的代数式表示NH3•H2O的电离常数Kb= .
(2)常温下,向一定体积的0.1mol•L﹣1醋酸溶液中加水稀释后,下列说法正确的是 .
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中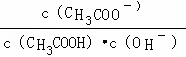 不变
不变
D.溶液中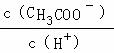 减小
减小
(3)①常温下将0.15mol•L﹣1的稀硫酸V1 mL与0.1mol•L﹣1的NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2= (溶液体积的变化忽略不计,硫酸电离方程式:H2SO4=2H++SO42﹣).
②常温下将pH=3的醋酸溶液V1 mL与pH=11的NaOH溶液V2 mL混合,则下列说法正确的是 .
A.若混合后溶液呈中性,则c(H+)+c(OH﹣)=2×10﹣7 mol•L﹣1
B.若V1=V2,混合后溶液的pH一定等于 7
C.若混合后溶液呈酸性,则V1一定大于V2
D.若混合后溶液呈碱性,则V1一定小于V2
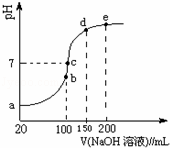
(4)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示.试分析图中a~e 5个点,回答下列问题:
①水的电离程度最大的是 点;
②在c点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组用铝片与稀硫酸反应制取氢气,以下能够加快该反应速率的是( )
①用浓硫酸代替稀硫酸
②加热
③改用铝粉
④增大稀硫酸的体积
⑤加水
⑥加入少量硫酸铜
A.全部 B.②③⑥ C.①②③⑥ D.②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式或叙述正确的是( )
A.1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642 kJ的热量:
N2H4(l)+O2(g)====N2(g)+2H2O(g) ΔH=+642 kJ·mol-1
B.12 g石墨转化为CO时,放出110.5 kJ的热量:
2C(石墨,s)+O2(g)====2CO(g) ΔH=-110.5 kJ·mol-1
C.已知:H2(g)+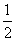 O2(g)====H2O(l) ΔH=-286 kJ·mol-1,
O2(g)====H2O(l) ΔH=-286 kJ·mol-1,
则:2H2O(l)====2H2(g)+O2(g)的ΔH=+572 kJ·mol-1
D.已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,
2NH3(g) ΔH=-92.4 kJ·mol-1,
则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com