
| A、标准状况下,1摩尔甲醇的体积约为22.4L |
| B、1摩尔庚烷中含有的共用电子对数为23摩尔 |
| C、1摩尔氢氧根离子(OH-)与羟基(-OH)所含电子数均为10NA |
| D、2.8 g乙烯与丙烯的混合物中含总原子的数目为0.6NA |


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
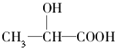 .已知有机物中若含有相同的官能团,则化学性质相似.完成下列问题:
.已知有机物中若含有相同的官能团,则化学性质相似.完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
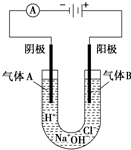 如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞.
如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞.查看答案和解析>>
科目:高中化学 来源: 题型:
A、Fe2O3+3CO
| ||||
| B、CO2+H2O═H2CO3 | ||||
C、CuO+H2
| ||||
D、2Na+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
| B、向溴化亚铁溶液中通入少量的Cl2:Cl2+2Br-═2Cl-+Br2 |
| C、向新制氯水中滴加NaOH溶液后,黄绿色褪去:Cl2+2OH-═ClO-+Cl-+H2O |
| D、将鸡蛋壳浸泡在盐酸中:CaCO3+2H+═Ca2++CO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤是由有机物和无机物组成的复杂的混合物 |
| B、医学上常用CuSO4溶液和NaOH溶液检验糖尿病人尿液中的葡萄糖 |
| C、反应物的总能量高于生成物的总能量时,发生吸热反应 |
| D、甲醛是某些劣质装饰板材释放的常见污染物之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、Na2O与盐酸反应:Na2O+2H+=2Na++H2O |
| C、向氢氧化钠溶液中通人过量C02:C02+OH-=HCO3- |
| D、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是将电能转化为化学能的装置 |
| B、由于生铁中含有碳,所以生铁比纯铁耐腐蚀 |
| C、在原电池中,电子从原电池的正极流向负极 |
| D、在原电池中,负极上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com