
”¾ĢāÄæ”æŅŃÖŖŌŚ25”ꏱ£¬“×Ėį”¢“ĪĀČĖį”¢Ģ¼ĖįŗĶŃĒĮņĖįµÄµēĄėĘ½ŗā³£Źż·Ö±šĪŖ£ŗ
“×ĖįK£½1.75”Į10£5
“ĪĀČĖįK£½2.95”Į10£8
Ģ¼ĖįK1£½4.30”Į10£7””K2£½5.61”Į10£11
ŃĒĮņĖįK1£½1.54”Į10£2””K2£½1.02”Į10£7
£Ø1£©Š“³öĢ¼ĖįµÄµŚŅ»¼¶µēĄėĘ½ŗā³£Źż±ķ“ļŹ½£ŗK1£½________”£
£Ø2£©Čō±£³ÖĪĀ¶Č²»±ä£¬ŌŚ“×ĖįČÜŅŗÖŠĶØČėÉŁĮæHCl£¬ĻĀĮŠĮæ»į±äŠ”µÄŹĒ________(Ģī×ÖÄø£¬ĻĀĶ¬)”£
a£®c(CH3COO£)””b£®c(H£«)””c£®“×ĖįµÄµēĄėĘ½ŗā³£Źż
£Ø3£©ĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ“ķĪóµÄŹĒ________”£
a£®ÉŁĮæCO2ĶØČė“ĪĀČĖįÄĘČÜŅŗÖŠ£ŗCO2£«H2O£«ClO£===![]() £«HClO
£«HClO
b£®ÉŁĮæSO2ĶØČė“ĪĀČĖįøĘČÜŅŗÖŠ£ŗCa2£«£«2ClO££«SO2£«H2O===CaSO3”ż£«2HClO
c£®¹żĮæCO2ĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ£ŗCO2£«OH£===![]()
”¾“š°ø”æ![]() a b
a b
”¾½āĪö”æ
(1)øł¾ŻµēĄėĘ½ŗā³£ŹżµÄŗ¬ŅåæɵĆĢ¼ĖįµÄµŚŅ»¼¶µēĄėĘ½ŗā³£Źż±ķ“ļŹ½K1=c(H+)c(HCO3-)/c(H2CO3)£»
(2)Čō±£³ÖĪĀ¶Č²»±ä£¬ŌŚ“×ĖįČÜŅŗÖŠĶØČėÉŁĮæHCl£¬a.CH3COO£»į½įŗĻH+ŠĪ³ÉCH3COOH£¬ĖłŅŌc(CH3COO£)±äŠ”£¬¹ŹaĻīÕżČ·£»
b.ÓÉÓŚ¼ÓČėĮĖH+£¬ĖłŅŌc(H£«)»įŌö“󣬹ŹbĻī“ķĪó£»
c.“×ĖįµÄµēĄėĘ½ŗā³£ŹżÖ»ÓėĪĀ¶ČÓŠ¹Ų£¬ĪĀ¶Č²»±ä£¬ĖłŅŌµēĄėĘ½ŗā³£Źż²»±ä£¬¹ŹcĻī“ķĪó£»
×ŪÉĻ£¬±¾ĢāŃ”a£»
(3)a.ÓÉÓŚĖįŠŌH2CO3>HClO> HCO3£,ĖłŅŌÉŁĮæCO2ĶØČė“ĪĀČĖįÄĘČÜŅŗÖŠ£¬»į·¢Éś·“Ó¦£ŗCO2£«H2O£«ClO£= HCO3££«HClO£¬¹ŹaĻīÕżČ·£»
b.ÓÉÓŚHClOÓŠĒæŃõ»ÆŠŌ£¬¶ųH2SO3ÓŠ»¹ŌŠŌ£¬ĖłŅŌÉŁĮæSO2ĶØČė“ĪĀČĖįøĘČÜŅŗÖŠ£¬»į·¢ÉśŃõ»Æ»¹Ō·“Ó¦£ŗCa2£«£«ClO££«SO2£«H2O=CaSO4”ż£«2H++Cl-,¹ŹbĻī“ķĪó£»
c.¹żĮæCO2ĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ£¬·¢Éś·“Ó¦µĆµ½æÉČÜŠŌĖįŹ½ŃĪ£¬Ąė×Ó·½³ĢŹ½ŹĒ£ŗCO2£«OH£= HCO3££¬¹ŹcĻīÕżČ·”£
×ŪÉĻ£¬±¾ĢāŃ”b”£


 Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬Ä³»ÆѧŠ”×éÄāÓĆøĆ×°ÖĆÖĘČ”“æ¾»µÄO2”£

(1)ČōCŹĒŅ»ÖÖµ»ĘÉ«¹ĢĢ壬ŌņÉÕĘæÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ___”£
(2)ČōCŹĒŅ»ÖÖŗŚÉ«·ŪÄ©£¬ŌņBŹĒ_________£¬CµÄ×÷ÓĆŹĒ________________”£
(3)¹ćæŚĘæÖŠŹ¢×°µÄŹŌ¼ĮDŹĒ___________£¬Ęä×÷ÓĆŹĒ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉč°¢·š¼ÓµĀĀŽ³£ŹżĪŖNA£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A.1molD2OĖłŗ¬ÖŹ×ÓŹżĪŖ12NA£»B.1molNa2O2Óė×ćĮæĖ®·“Ó¦×ŖŅʵē×ÓŹżĪŖ2NA£»
C.10g ÄŹĘųĖłŗ¬Ō×ÓŹżĪŖ0.5NA£»D.±źæöĻĀ22.4LÕżĪģĶéŗ¬ĒāŌ×ÓŹżĪŖ12NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĻĀĶ¼ĖłŹ¾£¬ĘäÖŠWŌ×ÓµÄÖŹ×ÓŹżŹĒĘä×īĶā²ćµē×ÓŹżµÄČż±¶£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©

A. Ō×Ó°ė¾¶£ŗW>Z>Y>X
B. ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ£ŗX>W>Z
C. ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗY>X>W>Z
D. ŌŖĖŲX”¢Z”¢WµÄ×īøß»ÆŗĻ¼Ū·Ö±šÓėĘäÖ÷×åŠņŹżĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫Ņ»¶ØĮæ°±»ł¼×Ėįļ§¼ÓČėŗćČŻČŻĘ÷ÖŠ£ŗNH2COONH4(s)![]() 2NH3(g)+CO2(g)”£øĆ·“Ó¦µÄĘ½ŗā³£ŹżµÄøŗ¶ŌŹż(-lgK)ÖµĖęĪĀ¶Č(T)µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
2NH3(g)+CO2(g)”£øĆ·“Ó¦µÄĘ½ŗā³£ŹżµÄøŗ¶ŌŹż(-lgK)ÖµĖęĪĀ¶Č(T)µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
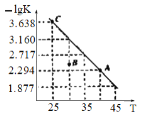
A. øĆ·“Ó¦µÄÉś³ÉĪļ×ÜÄÜĮæ“óÓŚ·“Ó¦Īļ×ÜÄÜĮæ
B. “¦ÓŚAµćµÄCO2µÄĻūŗÄĖŁĀŹ“óÓŚ“¦ÓŚCµćµÄCO2ĻūŗÄĖŁĀŹ
C. BµćŹ±£¬vÄę>vÕż
D. CO2µÄĢå»ż·ÖŹż²»±äŹ±·“Ó¦Ņ»¶Ø“ļµ½Ę½ŗāדĢ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē»Æѧ½µ½ā![]() µÄŌĄķČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
µÄŌĄķČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A. Ē¦Šīµē³ŲµÄøŗ¼«·“Ó¦ĪŖ£ŗPb - 2e£+ SO42- =PbSO4
B. µē½āŅ»¶ĪŹ±¼äŗó£¬Čō²»æ¼ĀĒČÜŅŗĢå»ż±ä»Æ£¬½»»»Ä¤×ó²ąČÜŅŗĖįŠŌŌöĒ棬ÓŅ²ąČÜŅŗĖįŠŌ¼õČõ
C. øƵē½ā³ŲµÄŅõ¼«·“Ó¦Ź½ĪŖ2NO3-+12H£«+10e£=N2”ü+6H2O
D. Čōµē½ā¹ż³ĢÖŠ×ŖŅĘ2mole££¬ŌņÖŹ×Ó½»»»Ä¤×ó²ąµē½āŅŗµÄÖŹĮæ¼õÉŁ¦¤m(×ó) =18.0g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éŅŌŃĒĻõĖįÄĘ£ØNaNO2£©ČÜŅŗĪŖŃŠ¾æ¶ŌĻó£¬Ģ½¾æNO2-µÄŠŌÖŹ”£
ŹµŃé | ŹŌ¼Į | ±ąŗż°ĻÖĻó | |
µĪ¹Ü | ŹŌ¹Ü | ||
2mL | 1%·ÓĢŖČÜŅŗ | 1 mol”¤L-1 NaNO2ČÜŅŗ | ŹµŃéI£ŗČÜŅŗ±äĪŖĒ³ŗģÉ«£¬Ī¢ČČŗóŗģÉ«¼ÓÉī |
1 mol”¤L-1 NaNO2ČÜŅŗ | 0.1 mol”¤L-1 KMnO4 ČÜŅŗ | ŹµŃéII£ŗæŖŹ¼ĪŽĆ÷ĻŌ±ä»Æ£¬ĻņČÜŅŗÖŠµĪ¼ÓĻ”ĮņĖįŗó×ĻÉ«ĶŹČ„ | |
KSCNČÜŅŗ | 1 mol”¤L-1 FeSO4 ČÜŅŗ£ØpH=3£© | ŹµŃéIII£ŗĪŽĆ÷ĻŌ±ä»Æ | |
1 mol”¤L-1 NaNO2ČÜŅŗ | 1 mol”¤L-1 FeSO4 ČÜŅŗ£ØpH=3£© | ŹµŃéIV£ŗČÜŅŗĻȱä»Ę£¬ŗóŃøĖŁ±äĪŖ×ŲÉ«£¬µĪ¼ÓKSCNČÜŅŗ±äŗģ | |
׏ĮĻ£ŗ[Fe(NO)]2+ŌŚČÜŅŗÖŠ³Ź×ŲÉ«”£
£Ø1£©½įŗĻ»ÆѧÓĆÓļ½āŹĶŹµŃéI”°Ī¢ČČŗóŗģÉ«¼ÓÉī”±µÄŌŅņ ______
£Ø2£©ŹµŃéIIÖ¤Ć÷NO2-¾ßÓŠ_____ŠŌ£¬ “ÓŌ×Ó½į¹¹½Ē¶Č·ÖĪöŌŅņ_________
£Ø3£©Ģ½¾æŹµŃéIVÖŠµÄ×ŲÉ«ČÜŅŗ
¢ŁĪŖČ·¶Ø×ŲÉ«ĪļÖŹŹĒNOÓėFe2+£¬¶ų·ĒFe3+·¢ÉśĀēŗĻ·“Ó¦µÄ²śĪļ£¬Éč¼ĘČēĻĀŹµŃ飬Ēė²¹ĘėŹµŃé·½°ø”£
ŹµŃé | ČÜŅŗa | ±ąŗż°ĻÖĻó |
| 1 mol”¤L-1FeSO4ČÜŅŗ£ØpH=3£© | i£®ČÜŅŗÓÉ___É«ŃøĖŁ±äĪŖ___É« |
____________________ | ii£®ĪŽĆ÷ĻŌ±ä»Æ |
¢Ś¼ÓČČŹµŃéIVÖŠµÄ×ŲÉ«ČÜŅŗ£¬ÓŠĘųĢåŅŻ³ö£¬øĆĘųĢåŌŚ½Ó½üŹŌ¹ÜæŚ“¦±äĪŖŗģ×ŲÉ«£¬ČÜŅŗÖŠÓŠŗģŗÖÉ«³ĮµķÉś³É”£½āŹĶÉĻŹöĻÖĻó²śÉśµÄŌŅņ_________”£
£Ø4£©ĀēŗĻ·“Ó¦µ¼ÖĀ·“Ó¦ĪļÅضČĻĀ½µ£¬øÉČÅŹµŃéIVÖŠŃõ»Æ»¹Ō·“Ó¦·¢Éś¼°²śĪļ¼ģŃ锣Š”×éĶ¬Ń§Éč¼ĘŹµŃéV£ŗ½«K±ÕŗĻŗóµēĮ÷±ķÖøÕė·¢ÉśĘ«×Ŗ£¬Ļņ×ó²ąµĪ¼Ó“×ĖįŗóĘ«×Ŗ·ł¶ČŌö“ó”£
¢ŁŃĪĒŵÄ×÷ÓĆŹĒ____________________________
¢Śµē³Ų×Ü·“Ó¦Ź½ĪŖ______________________
ŹµŃé½įĀŪ£ŗNO2-ŌŚŅ»¶ØĢõ¼žĻĀĢåĻÖŃõ»ÆŠŌ»ņ»¹ŌŠŌ£¬Ńõ»¹ŠŌĒæČõÓėČÜŅŗĖį¼īŠŌµČŅņĖŲÓŠ¹Ų”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉÄę·“Ó¦2NO2![]() 2N0+O2ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ£Ø £©
2N0+O2ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ£Ø £©
¢Łµ„Ī»Ź±¼äÄŚÉś³ÉnmolO2µÄĶ¬Ź±Éś³É2nmolNO2
¢Śµ„Ī»Ź±¼äÄŚÉś³ÉnmolO2µÄĶ¬Ź±Éś³É2nmolNO
¢ŪÓĆNO2”¢NO”¢O2µÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹµÄ±ČĪŖ2 : 2 : l µÄדĢ¬
¢Ü»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁøıäµÄדĢ¬
A. ¢Ł¢Ü B. ¢Ś¢Ū C. ¢Ł¢Ū¢Ü D. ¢Ł¢Ś¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņNaOHŗĶNa2CO3»ģŗĻČÜŅŗÖŠµĪ¼Ó0.1mol”¤L£1Ļ”ŃĪĖį£¬CO2µÄÉś³ÉĮæÓė¼ÓČėŃĪĖįµÄĢå»ż(V)µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©

A.ŌŚ0”«a·¶Ī§ÄŚ£¬Ö»·¢ÉśÖŠŗĶ·“Ó¦
B.a£½0.3
C.ab¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖCO32-£«2H£«=CO2”ü£«H2O
D.Ō»ģŗĻČÜŅŗÖŠNaOHÓėNa2CO3µÄĪļÖŹµÄĮæÖ®±ČĪŖ1”Ć2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com