
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:

实验步骤:
在A中加入4.4 g的异戊醇、6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是______。
(2)在洗涤操作中,第一次水洗的主要目的是____________,第二次水洗的主要目的是___________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后______(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是________________。
(5)实验中加入少量无水MgSO4的目的是___________。
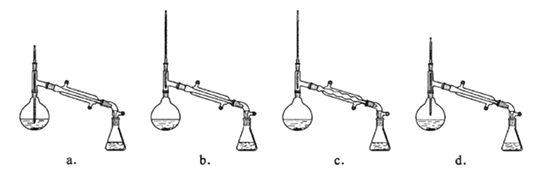
(6)在蒸馏操作中,仪器选择及安装都正确的是______(填标号)。
(7)本实验的产率是______(填标号)。
a.30℅ b.40℅ c.60℅ d.90℅
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏__(填“高”或“低”), 原因是_____________。
【答案】 球形冷凝管 洗掉大部分硫酸和醋酸 洗掉碳酸氢钠 d 提高醇的转化率 干燥乙酸异戊酯 b c 高 会收集少量未反应的异戊醇
【解析】试题分析:(1)由装置示意图可知装置B的名称是球形冷凝管;(2)反应后的溶液要经过多次洗涤,在洗涤操作中,第一次水洗的主要目的是除去大部分催化剂硫酸和未反应的反应物醋酸;用饱和碳酸氢钠溶液既可以除去未洗净的醋酸,也可以降低酯的溶解度;再第二次水洗,主要目的是洗去产品上残留的碳酸氢钠;(3)由于酯的密 度比水小,二者互不相溶,因此水在下层,酯在上层。分液时,要先将水层从分液漏斗的下口放出,待到两层液体界面时关闭分液漏斗的活塞,再将乙酸异戊酯从上口放出。因此选项是D。(4)酯化反应是可逆反应,增大反应物的浓度可以使平衡正向移动。增加一种反应物的浓度,可能使另一种反应物的转化率提高。因此本实验中加入过量乙酸的目的是提高醇的转化率;(5)实验中加入少量无水硫酸镁的目的是吸收酯表面少量的水分,对其减小干燥。(6)在蒸馏操作中,温度计的水银球要在蒸馏烧瓶的支管口附近。排除a、d,而在c中使用的是球形冷凝管,容易使产品滞留,不能全部收集到锥形瓶中,因此仪器选择及安装都正确的是b。 n(乙酸)="6.0g÷60g/mol" =0.1mol;n(异戊醇) =4.4g÷88g/mol=0.05mol。由于二者反应时是1:1反应的,乙酸过量,要按照醇来计算。n(乙酸异戊酯)=3.9g÷130g/mol=0.03mol。所以本实验的产率是0.03mol÷0.05mol×100℅=60℅。选项是D。(8)在进行蒸馏操作时,若从 130 ℃开始收集馏分,此时的蒸气中含有醇,会收集少量的未反应的异戊醇,因此产率偏高。


科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+B![]() C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
A. 若B是气体,增大A的浓度会使B转化率增大
B. 若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
C. 升高温度,C百分含量减少,说明正反应是放热反应
D. 增大压强,平衡不移动,说明B是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质间的反应与反应类型不相符的是( )
A.乙烯与溴水(加成反应)
B.甲苯与浓硝酸(硝化反应)
C.氯乙烷与氢氧化钠醇溶液 (取代反应)
D.乙烯与高锰酸钾(氧化反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)分离沸点不同但又互溶的液体混合物,常用的方法是 ;分离不溶性固体和液体混合物的常用的方法是 ;分离两种溶解度相差很大的溶质的溶液时,常用的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,请回答有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
(2)表中能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的单质与⑨最高价氧化物对应水化物反应的化学方程式 .
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入如表.
实验步骤 | 实验现象与结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃、l0lkPa条件下
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-2834.9kJ/mol
4Al(s)+2O3(g)=2Al2O3(s) ΔH=-3119.91kJ/mol: 由此得出的结论正确的是
A. 等质量的O2比O3能量低,由O2变O3为吸热反应
B. 等质量的O2比O3能量低,由O2变O3为放热反应
C. O3比O2稳定,由O2变O3为吸热反应
D. O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属说法正确的是
A. 自然界中的金属元素都以化合态存在
B. 金属钠着火,可以用水灭火
C. 铁在潮湿的空气中很稳定,但红热的铁丝可与水蒸气反应
D. Al与NaOH溶液的反应中,每转移3mole-,就生成1.5molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示. 已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差l.下列说法正确的是( ) 
A.Y、Z、W处于同一周期
B.X、Y、Z、W的原子序数递增
C.X、W可形成化学式为XW的离子化合物
D.简单离子半径是Z大于W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com