下列说法正确的是( )
A.水的沸点比硫化氢的高,是因为H2O分子内存在氢键,H2S分子内不能形成氢键
B.晶体中有阴离子则必然有阳离子,而有阳离子不一定有阴离子
C.金刚石的熔点比晶体硅高,是因金刚石为原子晶体而晶体硅为分子晶体
D.二氧化硅晶体的熔点较高,是因晶体中SiO2分子间的作用力较强
【答案】分析:A.O的电负性大,水分子间中含有氢键;
B.金属晶体中含有金属阳离子,没有阴离子;
C.C-C键长比Si-Si键长短;
D.二氧化硅晶体为原子晶体.
解答:解:A.因O的电负性大,水分子间中含有氢键,则水的沸点比硫化氢的高,是因为H2O分子之间存在氢键,H2S分子之间不能形成氢键,故A错误;
B.离子晶体中有阴离子则必然有阳离子,而金属晶体中含有金属阳离子,没有阴离子,故B正确;
C.C-C键长比Si-Si键长短,则金刚石的熔点比晶体硅高,金刚石、晶体硅都属于原子晶体,故C错误;
D.二氧化硅晶体为原子晶体,则由于Si-O键的键能大,所以二氧化硅晶体的熔点较高,故D错误;
故选B.
点评:本题考查晶体类型与氢键、物质的性质,明确常见晶体的构成微粒、熔沸点的比较方法、常见物质的氢键即可解答,难度不大.




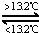 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,