
分析 粉末仅含Na、Fe、N、O四种元素.水溶性试验表明,固体粉末部分溶解,经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸,则该红棕色固体是氧化铁;取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L,则甲中含有两种元素,且甲是可溶性物质,加热时能分解生成氮气和单质,则甲是氮化钠,乙是钠,单质乙在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另一种单质,钠和氧化铁反应生成氧化钠和铁,所以丙是氧化钠,化合物丙与空气接触可转化为可溶性盐,过氧化钠和二氧化碳能反应生成可溶性盐,根据物质的性质来分析解答.
(1)根据题干信息推导出甲、乙、丙三种物质,由分解的甲的质量和产生的氮气体积确定甲的化学式;
(2)根据物质的性质来书写化学方程式;
(3)根据单质和红棕色粉末发生的置换反应来分析;
(4)根据红棕色粉末氧化铁的作用来寻找可替代的物质;
(5)根据可溶盐的可能组成情况结合盐的性质进行检验.
解答 解:(1)Na、Fe、N、O四种元素组成的化合物中为红棕色且可溶于盐酸的只有Fe2O3,在四种元素组成的单质中,可以在高温隔绝空气的条件下与Fe2O3反应的就只有金属钠了,因此单质乙是钠,化合物甲是由Na和N元素组成,13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L,即0.3mol,经计算知Na和N的原子个数比是1:3,所以化合物甲的化学式为NaN3,
故答案为:NaN3;
(2)因为丙是在高温隔绝空气的条件下生成的,在根据丙的性质可知丙只能是Na2O而不是Na2O2,反应的化学方程式为:Na2O+2CO2+H2O=2NaHCO3,
故答案为:Na2O+2CO2+H2O=2NaHCO3;
(3)钠和氧化铁发生的置换反应方程式为:6Na+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3Na2O,所以安全气囊中氧化铁粉末的作用是消耗产生的活泼的钠,避免分解产生的金属钠可能产生的危害,
故答案为:避免分解产生的金属钠可能产生的危害;
(4)安全气囊中氧化铁粉末的作用是消耗产生的活泼的钠,硝酸钾本身受热分解产生氧气,可以和金属钠反应,选项中能和钠反应的还有氧化铜,
故答案为:BD;
(5)氧化钠跟空气接触所得的可溶性的盐成分可能是Na2CO3,或NaHCO3,或Na2CO3与NaHCO3混合物,碳酸氢钠受热容易分解,碳酸钠受热稳定,故可以用加热的办法来确定成分,实验方案为:准确称取一定量的生成物.加热至恒重后,如果试样无失重,则为Na2CO3;如加热后失重,根据失重的量在试样总质量中的比例,即可推断出试样为NaHCO3,或Na2CO3与NaHCO3混合物,
故答案为:准确称取一定量的生成物.加热至恒重后,如果试样无失重,则为Na2CO3;如加热后失重,根据失重的量在试样总质量中的比例,即可推断出试样为NaHCO3,或Na2CO3与NaHCO3混合物.
点评 本题以推断题的形式考查学生元素和化合物的知识,明确物质的性质及其颜色是解本题关键,题目难度中等.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:解答题
 下表中实线表示目前元素周期表七个周期的部分边界. ①~⑧八种元素在周期表中的相对位置如下:
下表中实线表示目前元素周期表七个周期的部分边界. ①~⑧八种元素在周期表中的相对位置如下:
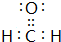 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 双酚A属于酚类 | B. | 双酚A属于芳香族化合物 | ||
| C. | 双酚A与苯酚互为同系物 | D. | 双酚A不属于醇类 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

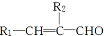 +H2O
+H2O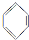 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$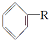 +HCl
+HCl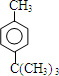 ;
;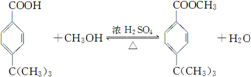 ;
;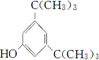 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中只含Fe3+、SO42-、Cl- | |
| B. | 溶液中只含Cu2+、SO42- | |
| C. | 需要利用焰色反应才能确定有无Na+ | |
| D. | 溶液中肯定没有I-但无法确定有无Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(葡萄糖)+6O2═6CO2+6H2O | B. | CH3COOH+KOH═CH3COOK+H2O | ||
| C. | 所有高温条件下发生的反应 | D. | C+CO2$\frac{\underline{\;\;△\;\;}}{\;}$2CO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com