
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键 ②共价化合物一定含共价键,也可能含离子键 ③含金属元素的化合物不一定是离子化合物 ④由非金属元素组成的化合物一定是共价化合物 ⑤由分子组成的物质中一定存在共价键 ⑥熔融状态能导电的化合物一定是离子化合物
A.①③⑤ B.②④⑥ C.②③④ D.①③⑥
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(1)氢氧燃料电池以KOH溶液作电解质溶液时,工作一段时间后,电解质溶液的浓度将________,溶液的pH____________________________。(填“减小”、“增大”或“不变”)
(2)氢氧燃料电池以H2SO4溶液作电解质溶液时,工作一段时间后,电解质溶液的浓度将________,溶液的pH________。(填“减小”、“增大”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp (25℃)如下:
| AgCl | AgI | Ag2S | |
| Ksp(单位省略) | 1.8×10-10 | 1.5×10-16 | 6.3×10-50 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀容易转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
为了综合利用副产品CaSO4,某化工厂与相邻的合成氨厂联合设计了下列(NH4)2SO4生产流程:
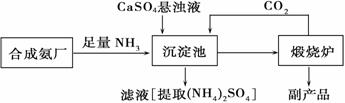
请回答以下问题:
(1)合成氨反应的化学方程式是 ,该反应在 (填设备名)中发生,反应所用催化剂一般用 。
(2)沉淀池中发生的主要反应方程式是 ,该反应能够发生的原因是 。
(3)在上述流程中可以循环使用的物质是 ,该生产过程中的副产品是 。
(4)从绿色化学和资源综合利用的角度说明上述流程的主要优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈醋酸逐渐凝固。下列说法正确的是
A、NH4HCO3与盐酸的反应是放热反应 B、该反应中,热能转化为产物内部的能量
C、反应物的总能量高于生成物的总能 D、该反应的反应物和生成物的能量高低与醋酸的凝固无关
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应4NH3(g)+5 O2 (g)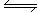 4NO (g)+6H2O (g)。回答下列问题:
4NO (g)+6H2O (g)。回答下列问题:
(1)在一定温度下,向一个5 L的密闭容器中充入0.20 mol的NH3和0.80 mol的O2,如反应初始6min内NH3的平均反应速率v(NH3)=0.003 mol·L-1·min-1,则6 min时c(O2)=___mol·L-1,NO的物质的量为________mol;反应一段时间后,达到平衡状态,如果这时向该密闭容器中再充入1 mol氩气,平衡时NH3的转化率________。(填“增大”“不变”或“减小”)
(2)判断该反应是否达到平衡的依据为________(填正确选项前的字母):a.体系压强不随时间改变 b.气体的密度不随时间改变 c.c(NH3)不随时间改变 d.单位时间里生成NO和H2O (g)的物质的量之比为4:6
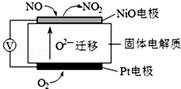 (3)氮的氧化物NOx是大气污染的主要污染物之一,通过NOx传感器可监测NOx的含量,其工作原理示意图如右:(工作原理和燃料电池类似)①Pt电极为 极(填正、负);NiO电极发生 反应(填“氧化”或“还原”).
(3)氮的氧化物NOx是大气污染的主要污染物之一,通过NOx传感器可监测NOx的含量,其工作原理示意图如右:(工作原理和燃料电池类似)①Pt电极为 极(填正、负);NiO电极发生 反应(填“氧化”或“还原”).
②写出NiO电极的电极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
通常状况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关 叙述正确的是( )
叙述正确的是( )
A.NCl3分 子中N—Cl键的键长比CCl4分子中C—Cl键的键长长
子中N—Cl键的键长比CCl4分子中C—Cl键的键长长
B.NCl3分子是非极性分子
C.分子中的所 有原子均达到8电子稳定结构
有原子均达到8电子稳定结构
D.NBr3比NCl3易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
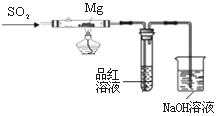 某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
实验Ⅰ 按右图所示进行实验。
(1)实验前需除去镁条表面氧化膜。用简易的物理
方法除氧化膜的操作是 ;
(2)实验室制取二氧化硫的化学方程式为 ;
(3)上述装置存在不合理之处,请提出1项改进建议 ;
 (4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
(4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
实验Ⅱ 确定固体M的成分。
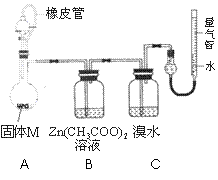
实验装置如右图所示。将分液漏斗中稀硫酸(足量)
加入到烧瓶中,完全反应后,实验现象如下:
|
(5)实验时,B装置中反应的化学方程式为 ;
(6)已知镁的相对原子质量为24,则固体M中金属镁的质量为 g;实验前装置内有空气,对金属镁质量的测定结果的影响是 (填偏低、偏高、无影响);
(7)依以上实验,可确定固体M的成分有 种(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2和Cl2均是常用的漂白剂,若将SO2和Cl2等物质的量混合后,先缓慢通入到BaCl2溶液中,再滴入品红试液,会观察到的现象是( )
A. 无沉淀生成,溶液显红色 B. 无沉淀生成,溶液显无色
C. 有沉淀生成,溶液显无色 D. 有沉淀生成,溶液显红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com