
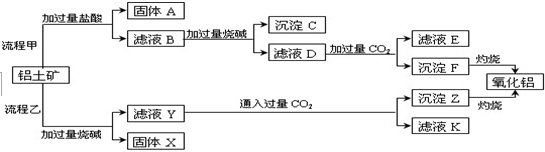
���� �����������ᷴӦ�ù���A����ҺB������AΪSiO2����ҺB�����Ȼ������Ȼ������Ȼ�þ�ȣ���Һ�м��������NaOH������֪����CΪ����������������þ����ҺD����ƫ�����ơ��Ȼ��ƣ���������ҺD��ͨ�����������̼��������������������̼�����ƣ�����FΪAl��OH��3����ҺE�к���NaCl��NaHCO3�����ݹ��������ҿ�֪���������е�Al2O3��SiO2�ܺ��������Ʒ�Ӧ����֪����XΪFe2O3��MgO�ȣ���ҺYΪ�����ơ�ƫ�����ƣ���Һ��ͨ�����������̼������ZΪAl��OH��3�����ᣬ��ҺK�к���NaHCO3���Դ˽����⣮
��� �⣺�����������ᷴӦ�ù���A����ҺB������AΪSiO2����ҺB�����Ȼ������Ȼ������Ȼ�þ�ȣ���Һ�м��������NaOH������֪����CΪ����������������þ����ҺD����ƫ�����ơ��Ȼ��ƣ���������ҺD��ͨ�����������̼��������������������̼�����ƣ�����FΪAl��OH��3����ҺE�к���NaCl��NaHCO3�����ݹ��������ҿ�֪���������е�Al2O3��SiO2�ܺ��������Ʒ�Ӧ����֪����XΪFe2O3��MgO�ȣ���ҺYΪ�����ơ�ƫ�����ƣ���Һ��ͨ�����������̼������ZΪAl��OH��3�����ᣬ��ҺK�к���NaHCO3��
��1�����̼������ᣬ��Ӧ���������ӵ�����Ϊ�������е�����������Ӧ�Ļ�ѧ����ʽΪ��Al2O3+6H+�T2Al3++3H2O��
�ʴ�Ϊ��Al2O3+6H+=2Al3++3H2O��
��2�������Ҽ���������������ƣ�����������Ӧ����ƫ�����ƣ���������跴Ӧ���ɹ����ƣ�����SiO32-�����ӷ���ʽΪ��SiO2+2OH-�TSiO32-+H2O��
�ʴ�Ϊ��SiO2+2OH-=SiO32-+H2O��
��3�����̼���HCl������FeCl3��MgCl2��AlCl3��Ҫ������ҺB�к���Fe3+�������ܶ࣬��ɼ���KSCN��ҺΪѪ��ɫ���뱽������ɫ����Ӧ����Fe��OH��3���ɫ����������֤����ҺB�к���Fe3+���ʴ�Ϊ�����軯�أ���������ء�������Һ�Ⱥ����𰸣���
��4�������Ϸ�����֪����AΪSiO2�������Ϸ�����֪��ҺE��K�����ʵ���Ҫ�ɷ���NaHCO3���ʴ�Ϊ��SiO2��NaHCO3��
���� ��������������ȡ��������Ϊ���忼�����ʵķ��롢�ᴿ�Լ��Ʊ���Ϊ�߿��������ͣ�������ѧ���ķ�����ʵ�������Ŀ��飬��Ŀ���ؿ��鿼�������ƶϡ�Ԫ�ػ��������ʼ��ת�������ӵķ��������ӷ���ʽ�ȣ��Ѷ��еȣ�ע�����ӷ���ʽ�����йأ�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 5�� | C�� | 6�� | D�� | 7�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.46 g | B�� | 3.20 g | C�� | 3.59 g | D�� | 7.41 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

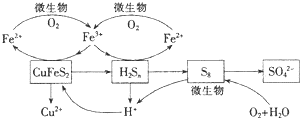
| A�� | ��CuFeS2����Cu2S��SO2�����������ﷴӦ����Ԫ�ر���ԭ | |
| B�� | ���������е���Ҫ��ӦΪ��Cu2S+O2$\frac{\underline{\;����\;}}{\;}$2Cu+SO2 | |
| C�� | ͭ�ĵ�⾫�������д�ͭ������ | |
| D�� | ����ұ�����̲�������SO2��ͨ���ñ���NaHSO3��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2����������ЧӦ����һ�ִ�����Ⱦ�� | |
| B�� | ����һ�ֻ�ɫ���壬������ˮ�����ھƾ� | |
| C�� | SO2��ʹƷ����Һ��ɫ����Ϊ������Ư���� | |
| D�� | NO2��SO2����Ҫ�Ĵ�����Ⱦ�����ˮ������γ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com