
| A、使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素 |
| B、将混有乙烯的乙烷气体通入酸性高锰酸钾溶液,可得到纯净的乙烷气体 |
| C、将苯与溴水混合后,再加铁粉,即可制得溴苯 |
| D、在蔗糖溶液中加入几滴稀硫酸,水浴加热5 min,加入NaOH溶液至碱性,再加入银氨溶液并水浴加热 |


科目:高中化学 来源: 题型:
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 甲 | 55 | SO2 | II | 良 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 | B、氯化钾溶液 |
| C、硝酸银溶液 | D、硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X和Y可能都是固体 |
| B、X和Y一定都是气体 |
| C、若Y为固体,X一定是气体 |
| D、X和Y不可能都是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若开始通入3mol A和3mol B,达到平衡后将生成3a mol C | ||
| B、若开始通入3mol A、2mol B和1mol C,达到平衡后密闭容器中C的物质的量可能为3mol | ||
| C、若开始时通入2mol A、2mol B和1mol C,达到平衡时,B的物质的量一定小于2mol | ||
D、若开始时通入2molA、2mol B和1mol C,达到平衡后,再通入2 mol C,则再次到达平衡后,C的物质的量分数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸 | B、硫酸 | C、硝酸 | D、王水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验SO42-的试剂是HCl和BaCl2 |
| B、检验Cl-的试剂是AgNO3和HNO3 |
| C、向溶液中加入BaCl2后生成白色沉淀,即证明有SO42- |
| D、检验CO32-的试剂HCl,澄清的石灰水,和CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
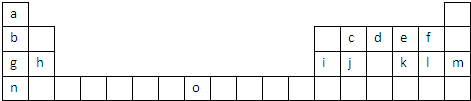
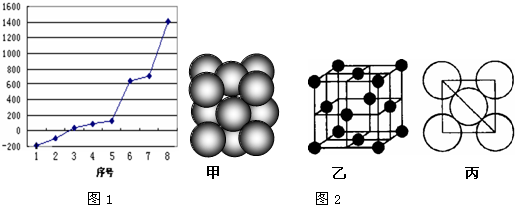
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com