
| A. | X元素可以与W元素形成WX2和WX3两种化合物 | |
| B. | Y元素的单质一定条件下可以与O2、N2、CO2反应 | |
| C. | Z原子的最外层电子数为4,形成化合物时一般为+4价 | |
| D. | X与Y、Z与W都属于同一周期 |
分析 短周期(前三周期)元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,则X有2个电子层,最外层电子数为6,故X为O元素;Y原子的最外层只有2个电子,Y应为第三周期的Mg元素;Z单质可制成半导体材料,则Z为Si元素;W与X属于同一主族,W为S,然后结合元素化合物知识来解答.
解答 解:短周期(前三周期)元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,则X有2个电子层,最外层电子数为6,故X为O元素;Y原子的最外层只有2个电子,Y应为第三周期的Mg元素;Z单质可制成半导体材料,则Z为Si元素;W与X属于同一主族,W为S,
A.X元素可以与W元素形成SO2和SO3两种化合物,故A正确;
B.Y元素的单质一定条件下可以与O2、N2、CO2反应,分别生成MgO、Mg3N2、MgO和C,故B正确;
C.Z原子的最外层电子数为4,形成化合物时一般为+4价,如SiO2、SiCl4中Si为+4价,故C正确;
D.由上述分析可知,X为第二周期元素,Y、Z、W均在第三周期,故D错误;
故选D.
点评 本题考查原子结构和周期律的应用,为高频考点,把握X原子的最外层电子数是其电子层数的3倍推断X为O元素为解答的关键,侧重分析与应用能力的考查,注意周期律及元素化合物知识运用,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性高锰酸钾褪色的原理和使溴水褪色的原理相同 | |
| B. | 乙烯不能合成高分子化合物 | |
| C. | 工业制备乙烯通常通过石油的裂解 | |
| D. | 聚乙烯能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子 | |
| B. | NH3和CH4的空间构型相似 | |
| C. | BF3与 都是平面型分子 都是平面型分子 | |
| D. | CO2和H2O都是直线型分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2与NO2 | B. | SO2与N2O | C. | SO2与O3 | D. | PCl3与BF3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ K+ OH- Cl- | B. | Na+ Cu2+ SO42- NO3- | ||
| C. | K+ Na+ SO42- Cl- | D. | Ba2+ CO32- NO3- K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 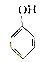 | B. | CH2═CH-Cl | ||
| C. | 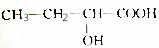 | D. | HO(CH2)4COOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com