
| A�� | ��KIO3����������Һ�е�KI��5I-+IO3-+3H2O�T3I2+6OH- | |
| B�� | ��NaAlO2��Һ��ͨ�������CO2��2AlO2-+CO2+3H2O�T2Al��OH��3��+CO32- | |
| C�� | ��SO2ͨ������䰱ˮ�У�SO2+NH3•H2O�THSO3-+NH4+ | |
| D�� | ��ˮ��ͨ��������SO2��I2+SO2+2H2O�T2I-+SO42-+4H+ |
���� A��������Һ�У���Ӧ�����в����������������ӣ�
B��������̼��������Ӧ����̼��������ӣ�
C����ˮ��������Ӧ��������������ӣ�
D���ⵥ�ʽ������������������ᣮ
��� �⣺A����KIO3����������Һ�е�KI�����߷���������ԭ��Ӧ���ɵⵥ�ʣ���ȷ�����ӷ���ʽΪ��5I-+IO3-+6H+�T3I2+3H2O����A����
B����NaAlO2��Һ��ͨ�������CO2����Ӧ������������������̼�����ƣ���ȷ�����ӷ���ʽΪ��AlO2-+CO2+2H2O�TAl��OH��3��+HCO3-����B����
C����SO2ͨ������䰱ˮ�У���Ӧ����������泥���ȷ�����ӷ���ʽΪ��SO2+2NH3•H2O�TSO32-+2NH4++H2O����C����
D����ˮ��ͨ��������SO2�����߷���������ԭ��Ӧ����HI�����ᣬ��Ӧ�����ӷ���ʽΪ��I2+SO2+2H2O�T2I-+SO42-+4H+����D��ȷ��
��ѡD��
���� ���⿼�������ӷ���ʽ����д�жϣ�Ϊ�߿��ĸ�Ƶ�⣬��Ŀ�ѶȲ���ע��������ȷ���ӷ���ʽ�����жϳ��÷�������鷴Ӧ��������Ƿ���ȷ���������ʲ���Ƿ���ȷ���������������ʵ���Ҫ������ѧʽ������Ƿ����ԭ��ѧ����ʽ�ȣ�


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ǧ���صķŵ練Ӧ | B�� | �����������ڸ����µķ�Ӧ | ||
| C�� | ������ˮ�ⷴӦ | D�� | ̿��CO2�Ļ��Ϸ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
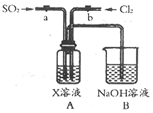 �����ͼװ��̽���������������Ļ�ѧ����ͨ�����Ƶ��ɼ�a��b����װ��A�зֱ�ͨ�벻ͬ���壬������������⣺
�����ͼװ��̽���������������Ļ�ѧ����ͨ�����Ƶ��ɼ�a��b����װ��A�зֱ�ͨ�벻ͬ���壬������������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���ܱ������з�����Ӧ��X+2Y?2Z����H��0��������Z����̬����Z��ƽ�������е����������Z%�����¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ���ǣ�������
���ܱ������з�����Ӧ��X+2Y?2Z����H��0��������Z����̬����Z��ƽ�������е����������Z%�����¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ���ǣ�������| A�� | Yһ������̬ | |
| B�� | T1����T2 | |
| C�� | �����¶ȣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������ | |
| D�� | ��c��X����c��Y����c��Z��=1��2��2ʱ����Ӧ�ﵽƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��չ������ͨ��ɫ���� | B�� | ���ȿ�����Դ�ٽ����÷�չ | ||
| C�� | ú̿ȼ��ʱ��װ������װ�� | D�� | �������������з��ദ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+ | B�� | NH4+ | C�� | CO32- | D�� | Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | C50H80 | B�� | C50H82 | C�� | C50H84 | D�� | C50H86 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com