


科目:高中化学 来源: 题型:
| A、在标准状况下,28g的N2和CO的混合气体,其体积约为22.4L |
| B、1molH2所占的体积一定是22.4L |
| C、在标准状况下,1mol水的体积约为22.4L |
| D、在标准状况下,NA个任何分子所占的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中只含有Cl2和H2O分子 |
| B、加入AgNO3溶液有白色沉淀产生 |
| C、光照氯水有气泡逸出,久置的氯水,酸性增强 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气溶于水 | |||
| B、氨气溶于水 | |||
C、可充电电池的反应如2Ag+Zn(OH)2
| |||
| D、工业合成氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
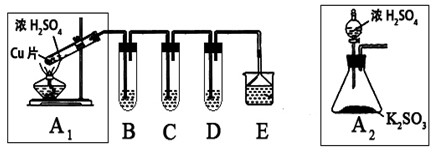
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 | |
| 步骤3: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com