
【题目】根据下列实验操作,回答问题:
(1)将在空气中久置的铝箔放在酒精灯火焰上加热,观察到的现象是_________________,上述变化的原因是______________。
(2)将用砂纸仔细打磨过的铝箔放在酒精灯火焰上加热,观察到的现象是_________________,上述变化的原因是____________________。
(3)将铝箔在氧气中点燃,观察到的现象是__________,反应的化学方程式是_______。
【答案】铝箔熔化,失去光泽,熔化的铝不滴落 构成铝表面氧化膜的氧化铝熔点很高(比铝高),包在铝的外面,使液态铝不能滴落 铝箔熔化,失去光泽,熔化的铝不滴落 加热时,铝先与氧气反应,生成的氧化铝包在铝的外面,使液态铝不能滴落 铝箔剧烈燃烧,发出耀眼的白光 4Al+3O2![]() 2Al2O3
2Al2O3
【解析】
(1)铝箔熔化,失去光泽,熔化的铝不滴落,是因为构成铝表面氧化膜的氧化铝熔点很高(比铝高),包在铝的外面,使液态铝不能滴落;答案:铝箔熔化,失去光泽,熔化的铝不滴落;构成铝表面氧化膜的氧化铝熔点很高(比铝高),包在铝的外面,使液态铝不能滴落。
(2) 铝箔熔化,失去光泽,熔化的铝不滴落,是因为铝是活泼金属,加热时,铝先与氧气反应,生成的氧化铝包在铝的外面,使液态铝不能滴落;答案:铝箔熔化,失去光泽,熔化的铝不滴落 ;加热时,铝先与氧气反应,生成的氧化铝包在铝的外面,使液态铝不能滴落;
(3)铝箔在氧气中剧烈燃烧,发出耀眼的白光,反应方程式为:4Al+3O2![]() 2Al2O3;
2Al2O3;
答案:铝箔剧烈燃烧,发出耀眼的白光; 4Al+3O2![]() 2Al2O3。
2Al2O3。


科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) ![]()
![]() N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g);ΔH= -373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在27.5 g水中溶解12.5 g CuSO45H2O,恰好达到饱和,该溶液密度为1.18 g·cm-3,求:
(1)该溶液中阴阳离子的总物质的量._________________
(2)该溶液中CuSO4的物质的量浓度(保留二位小数)。________________
(3)取出20.0 mL该溶液,加入足量Ba(OH)2溶液,反应后可得到沉淀质量多少克?(保留一位小数)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于 的说法,不正确的是
的说法,不正确的是
A.该物质能发生加成、氧化、聚合等反应
B.该物质苯环上的一氯取代有4种同分异构体
C.该物质在酸性条件下水解产物之一可用于合成阿司匹林
D.1mol该物质与足量NaOH溶液反应,最多可消耗5molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,已知∶CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g),下列说法不正确的是( )
CO2(g)+3H2(g),下列说法不正确的是( )
A.0.1 mol CH3OH中含共价键数为0.5NA
B.10.0g 质量分数为32%的CH3OH溶液与4.6g的钠反应,产生H2分子数为0.1NA
C.1 mol CH3OH与足量的H2O反应,得到CO2分子数为NA
D.每消耗0.1 mol CH3OH时,转移电子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。……
请回答下列问题(提示B分液漏斗中为浓氨水,滴入烧瓶可产生氨气):
(1)装置的连接顺序是:(a)接________,________接________;(b)接________

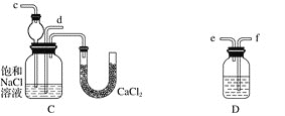
(2)A中常选用的固体反应物为______________;D中应选用的液体为________________(填化学式)。
(3)第二步骤中必须先让__________装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是______________________________,C中广口瓶内产生固体的总化学方程式为______________________ 。
(5)在第四步中分离NH4Cl晶体的操作是____________________(填操作名称);其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3(约占5%~8%),请设计一个简单的实验证明所得固体的成分中含有Na+,简要写出操作和现象____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过硝酸钠(NaNO4)能与水发生反应∶NaNO4+H2O= NaNO3+H2O2,下列说法不正确的是( )
A.过硝酸钠可用于杀菌消毒
B.过硝酸钠中含有-O-O-结构
C.过硝酸钠具有强氧化性,没有还原性
D.将过硝酸钠加入酸性FeSO4溶液中发生的离子方程式∶![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用下列实验装置或方案能达到实验目的的是
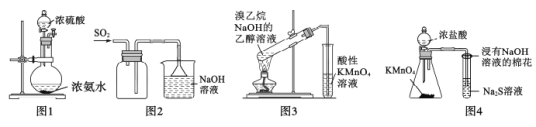
A.用图1装置制备少量氨气
B.用图2所示装置收集SO2
C.用图3所示装置检验是否有乙烯产生
D.用图4装置比较KMnO4、C12、S的氧化性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com