
【题目】碳酸锶(SrCO3)可用于制造彩电阴极射线管、荧光玻璃等。以天青石(主要含有SrSO4和少量MgCO3杂质)为原料生产SrCO3的流程如图:
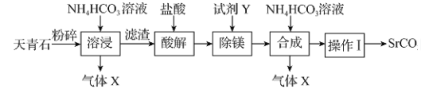
下列说法错误的是( )
A.锶的金属性比钙的强,所以SrSO4的溶解性比CaSO4的强
B.气体X和SO2均为酸性氧化物,且均能使紫色石蕊试液变红
C.“除镁”时,试剂Y可以选用苛性钠
D.“操作I”的母液经蒸发浓缩、冷却结晶可得到铵态氮肥
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:配制50 mL 0.001 mol/L FeCl3溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴1 mol/L HCl溶液、1滴1 mol/L NaOH 溶液,测得溶液pH随时间变化的曲线如下图所示。
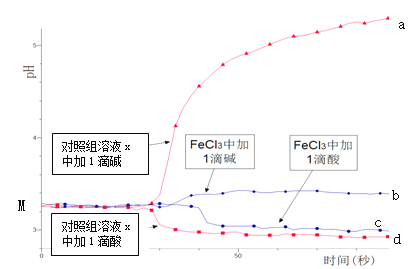
下列说法不正确的是
A.依据M点对应的pH,说明Fe3+发生了水解反应
B.对照组溶液x的组成可能是0.003 mol/L KCl
C.依据曲线c和d说明Fe3+水解平衡发生了移动
D.通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应2A(g)![]() B(g) ΔH>0在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的
B(g) ΔH>0在密闭容器中达到平衡,平衡后c(A)/c(B)=a,若改变某一条件,足够时间后反应再次达到平衡状态,此时c(A)/c(B)=b,下列叙述正确的
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B.在该温度恒压条件下再充入少量B气体,则a=b
C.若其他条件不变,升高温度,则a<b
D.若保持温度、压强不变,充入惰性气体,则a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
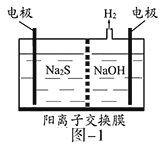
(1)将烧碱吸收H2S后的溶液加入到如题图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e-=S(n—1)S+ S2-=Sn2-。
①写出电解时阴极的电极反应式:__________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成_____________。
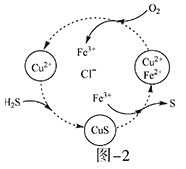
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如题图—2所示。
①在图示的转化中,化合价不变的元素是___________。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为_______________。
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有___________________。
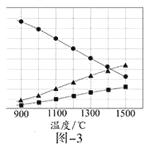
(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题图—3所示,H2S在高温下分解反应的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解100mL含c(H+)=0.3mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是( )
A. 0.10mol/LAg+B. 0.20mol/LZn2+C. 0.20mol/LCu2+D. 0.20mol/LPb2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮与氟、硫、镓三种元素之间可以形成具有特殊组成和性质的化合物。回答下列问题:
(1)基态镓原子电子排布式为___;硫原子核外有___种运动状态不同的电子。
(2)第一电离能符号为I1,I1(N)___I1(S)(填“>”或“<”)。
(3)NSF(N=S-F)与SNF(S=N-F)互为同分异构体。
①关于NSF与SNF的说法正确的是___ (填标号)。
A.二者均含有极性键和非极性键
B.二者均含有σ键与π键
C.二者均为非极性分子
D.二者与SO2均互为等电子体
②NSF发生聚合生成三聚分子A(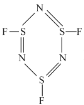 ),SNF发生聚合生成三聚分子B(
),SNF发生聚合生成三聚分子B(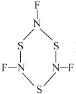 ),分子A中σ键与π键数目之比为___,分子B中氮原子价电子空间构型为___。
),分子A中σ键与π键数目之比为___,分子B中氮原子价电子空间构型为___。
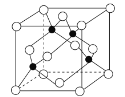
(4)氮化镓是直接隙半导体材料,具有易发光、电光转化效率高的特点。某种立方晶型氮化镓晶胞如图所示。(图中“O”与“●”大小比例关系符合二者原子实际大小比例关系)
①图中“●”表示的原子为___ (填元素符号)。
②已知NA为阿伏加德罗常数的值,晶胞的密度为dg·cm-3。则晶胞的边长为___ nm。两个距离最近的氮原子之间的距离为___ nm。(均用含d和NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是

A.烧瓶中立即出现白烟
B.烧瓶中立即出现红棕色
C.烧瓶中发生的反应表明常温下氨气有还原性
D.烧杯中的溶液是为了吸收有害气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的判断或表示方法正确的是
A.相同条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多
B.从C(石墨)=C(金刚石) △H=+1.9 kJ·mol-1,可知相同条件下金刚石比石墨更稳定
C.由H+(aq)+OH-(aq)= H2O(l) △H=-57.3 kJ·mol-1,可知:含1 molCH3COOH的稀溶液与含1 molNaOH的稀溶液混合,放出的热量大于57.3 kJ
D.2gH2完全燃烧生成液态水放出285.8kJ热量,则表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)= 2 H2O(l) △H=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3—环己二酮(![]() )常用作医药中间体,用于有机合成。1,3—环己二酮的一种合成路线如图所示。
)常用作医药中间体,用于有机合成。1,3—环己二酮的一种合成路线如图所示。
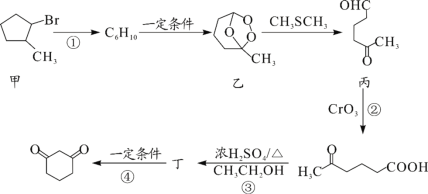
回答下列问题:
(1)甲的分子式为___。
(2)丙中含有官能团的名称是___。
(3)反应①所需的试剂和条件是___;②的反应类型是___。
(4)丁的结构简式为___。
(5)写出丙与新制氢氧化铜悬浊液反应的化学方程式___。
(6)符合下列条件的乙的同分异构体共有___种。
①能发生银镜反应
②能与NaHCO3溶液反应
其中核磁共振氢谱峰面积之比为1∶1∶2∶6的一种同分异构体的结构简式为___(任写一种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com