
SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则图中右侧Y形管中放置的药品组合符合要求的是(必要是可以加热)
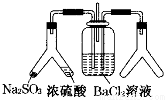
①Cu和浓硝酸 ②CaO和浓氨水 ③大理石和稀盐酸
④高锰酸钾溶液和浓盐酸 ⑤过氧化钠和水
A.只有①② B.只有③⑤ C.只有①②③ D.只有①②④⑤
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试理化学试卷(解析版) 题型:选择题
将某有机物完全燃烧,生成CO2和H2O。将12 g该有机物完全燃烧的产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,又增重26.4g。该有机物的分子式为
A.C4H10 B.C2H6O C.C3H8O D.C2H4O2
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
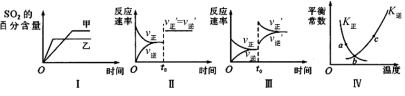
A.图I表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:填空题
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为 ,四氧化三铁可写成FeO·Fe2O3 的形式,如果将Pb3O4也写成相对应的形式应为: 。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为: 。
PbO2可有PbO与次氯酸钠溶液反应制得,其反应的离子方程式为 。
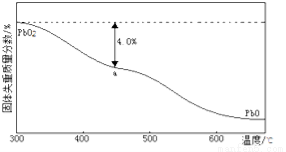
(3)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%(即 )的残留固体,若a点固体组成表示为PbO2或mPbO2 ·nPbO,计算x值和m:n , 。
)的残留固体,若a点固体组成表示为PbO2或mPbO2 ·nPbO,计算x值和m:n , 。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:填空题
化合物H可用以下路线合成:
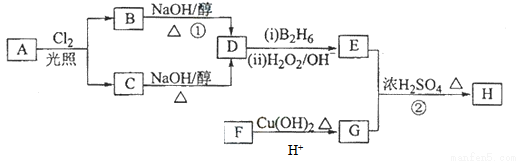
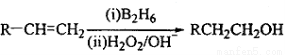
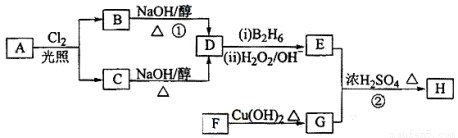 已知:
已知: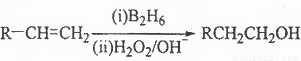
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以生成88gCO2和45gH2O,且A分子结构中有3个甲基,则A的名称(系统命名)为 ;
(2)B和C均为一氯代烃,则反应(1)的反应类型为 ;
(3)在催化剂存在下1molF与2molH2反应,生成3—苯基—1—丙醇。F的结构简式 。
(4)反应②的化学方程式为 ;
(5)与G具有相同官能团的芳香类同分异构体共有 种(不包括G),写出其中任意两种_____________、___________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷(解析版) 题型:选择题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是
A.XZ2、X2M2、M2Z2均为直线型的共价化合物
B.由X元素形成的单质不一定是原子晶体
C.原子半径:Z>Y>X
D.由Z、W两种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古巴彦淖尔市高三上期中考试理化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.干冰、液态氯化氢都是电解质
B.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
C.Na2O、Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物
D.Na2O2晶体中既含有离子键又含有共价键
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上学期期中考试化学试卷(解析版) 题型:选择题
利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。则下列说法不正确的是 ( )
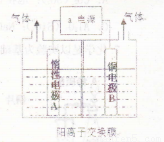
A.外加电源的a极为正极
B.电解过程中,Li+向B极迁移
C.阳极反应式为:4OH--4e-=O2↑+H2O
D.每生成1molLiOH,外电路转移1mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表.下列说法正确的是
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表.下列说法正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣5mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com