
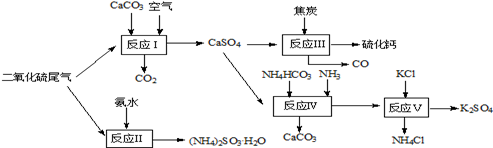
| A.滴有酚酞的NaOH溶液 | B.酸性KMnO4 |
| C.滴有淀粉的碘水 | D.BaCl2溶液. |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:不详 题型:单选题
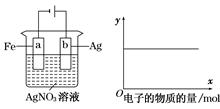
| A.①③ | B.③④ | C.①②④ | D.①②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
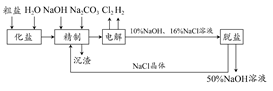
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | a | b | c | d |
| A | Pt | Pt | NaOH | NaOH |
| B | C | C | NaCl | NaOH |
| C | Cu | Cu | CuSO4 | Cu(OH)2 |
| D | Pt | Pt | H2SO4 | H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
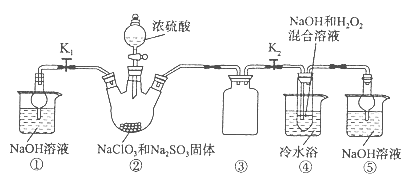
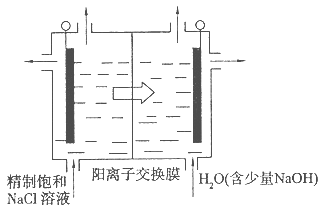
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuCl2 (CuO) | B.NaOH (NaOH) |
| C.CuSO4 (CuCO3) | D.NaCl (NaOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.阴极:2H++2e- H2↑阳极:4OH--4e- H2↑阳极:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
B.阴极:2H++2e- H2↑ 阳极:2Cl--2e- H2↑ 阳极:2Cl--2e- Cl2↑ Cl2↑ |
C.阴极:Cu2++2e- Cu阳极:4OH--4e- Cu阳极:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
D.阴极:Cu2++2e- Cu 阳极:2Cl--2e- Cu 阳极:2Cl--2e- Cl2↑ Cl2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH | B.H2SO4 | C.AgNO3 | D.Na2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com