
| A. | M原子所含质子数一定大于R原子所含质子数 | |
| B. | M、R两种元素结合形成的化合物中不可能含有共价键 | |
| C. | M2-与R+的电子层结构不可能相同 | |
| D. | M一定存在同素异形体 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 56a L | B. | (a+b)mol | C. | 56b L | D. | (a+b)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
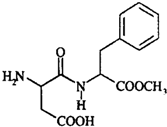 阿斯巴甜具有清爽的甜味,甜度约为蔗糖的200倍,其结构简式如图所示.下列关于阿斯巴甜的说法错误的是( )
阿斯巴甜具有清爽的甜味,甜度约为蔗糖的200倍,其结构简式如图所示.下列关于阿斯巴甜的说法错误的是( )| A. | 阿斯巴甜属于糖类 | |
| B. | 在一定条件下完全水解,产物中有两种氨基酸 | |
| C. | 既能与酸反应又能与碱反应 | |
| D. | 可发生取代反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖和麦芽糖是互为同分异构体,不是同系物 | |
| B. | 油脂、糖类和蛋白质在一定条件都能发生水解反应 | |
| C. | 淀粉和纤维素的水解产物都可以发生银镜反应 | |
| D. | 蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
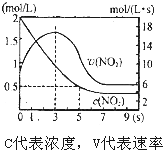
| A. | 5s 时NO2的转化率为75% | |
| B. | 0-3s 时v(NO2 )增大是由于体系温度升高 | |
| C. | 3s 时化学反应处于平衡状态 | |
| D. | 9s 时再充入N2O4,平衡后平衡常数K 较第一次平衡时大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Li<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性:H2SO4<H2CO3<HNO3 | D. | 沸点:H2O>H2S>H2Se |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,24g O3与11.2LO2所含的分子数一定相等 | |
| B. | lmol.L-1的AlCl3溶液中含有Cl-的个数为3NA | |
| C. | 标准状况下,22.4L氯气与足量铁粉充分反应,转移的电子数为2NA | |
| D. | 密闭容器中加入l.5molH2和0.5molN2,充分反应后可得NH3分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com