
| A. | SO42- | B. | HCO3- | C. | SO32- | D. | Br- |
分析 通入Cl2后溶液中含盐酸、HClO,具有酸性和强氧化性,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,不能发生氧化还原反应,则离子浓度不减小,以此来解答.
解答 解:通入Cl2后溶液中含盐酸、HClO,具有酸性和强氧化性,
A.能氧化SO32-生成SO42-,则SO42-浓度增大,故A正确;
B.盐酸与HCO3-反应,离子浓度减小,故B错误;
C.能氧化SO32-生成SO42-,则SO32-浓度减小,故C错误;
D.Br-被氧化成溴单质,导致Br-的浓度减小,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应及复分解反应的离子共存考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 氯原子的电子排布式3s23p5 | B. | Cl-的结构示意图  | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热.冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证AgI的溶解度小于AgCl | 将NaI浓溶液加入AgCl悬浊液中,振荡,可观察到沉淀由白色变为黄色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向铝盐溶液中不断加入小苏打 | B. | 向偏铝酸钠溶液中不断滴加盐酸 | ||
| C. | 向烧碱溶液中不断滴入铝盐溶液 | D. | 向铝盐溶液中不断滴入烧碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
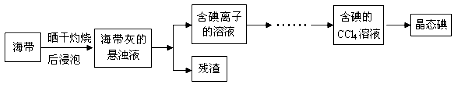
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO-、K+、Cl- | B. | Ba2+、Na+、Br- | C. | Na+、Fe3+、SO42- | D. | K+、NO3-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Cl2中的HCl:将混合气体通过AgNO3溶液 | |
| B. | 除去C2H6中的C2H4:将混合气体通过酸性KMnO4溶液 | |
| C. | 检验CO2中是否混有HCl:将气体通入饱和NaHCO3溶液 | |
| D. | 检验Cl2中是否混有空气:将装有气体的试管倒置在NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D |
| 性质 结构 信息 | 单质银白色,燃烧时火焰呈黄色. | 其单质是空气的主要成分,化学性质非常稳定. | 原子的3p亚层上有5个电子. | +2价阳离子的核外电子排布与氖原子相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
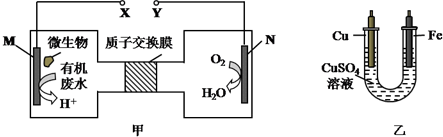
| A. | 乙装置中溶液颜色会变浅 | |
| B. | 铁电极应与Y相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25mol气体时,则铜电极质量减少16g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com