
下列溶液中微粒的物质的量浓度关系正确的是( )
A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4溶液:c(NH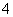 )大小顺序为①>②>③
)大小顺序为①>②>③
B.0.2 mol·L-1CH3COOH溶液和0.2 mol·L-1CH3COONa溶液等体积混合:c(CH3COOH)+c(H+)-c(OH-)=0.1 mol·L-1
C.0.1 mol·L-1 NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)=c(HCO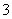 )+c(CO
)+c(CO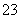 )+c(OH-)
)+c(OH-)
D.0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
已知 (l)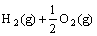 =H2O(g) ; △H1=a kJ·
=H2O(g) ; △H1=a kJ·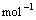
(2)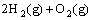 =2H2O(g) ; △H2=b kJ·
=2H2O(g) ; △H2=b kJ·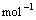
(3)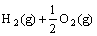 =H2O(l) ; △H3=c kJ·
=H2O(l) ; △H3=c kJ·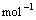
(4)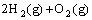 =2H2O(l) ; △H4=d kJ·
=2H2O(l) ; △H4=d kJ·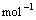
下列关系式中正确的是 ( )
A.a<c <0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
某可逆反应L(s)+G(g)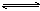 3R(g) △H>0,右图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示
3R(g) △H>0,右图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示
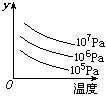 A.平衡混合气中R的质量分数 B.达到平衡时G的转化率
A.平衡混合气中R的质量分数 B.达到平衡时G的转化率
C.平衡混合气中G的质量分数 D.达到平衡时L的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如下图所示(某些条件和部分产物已略去)。下列说法不正确的是( )
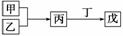
A.若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物
B.若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙可能为Na2O2
C.若丙、丁混合产生白烟,且丙分子为18电子分子,丁分子为10电子分子,则乙的水溶液可能具有漂白作用
D.若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序一定为甲<丙<戊
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的转化在给定条件下能实现的是( )
A.NaAlO2(aq)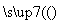 AlCl3
AlCl3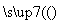 Al
Al
B.NH3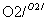 NO
NO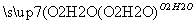 HNO3
HNO3
C.NaCl(饱和)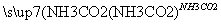 NaHCO3
NaHCO3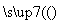 Na2CO3
Na2CO3
D.FeS2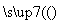 SO3
SO3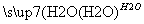 H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,0.1 mol Na2CO3与盐酸混合得到一组体积为1 L的溶液,溶液中部分微粒与pH的关系如图所示,下列有关溶液中离子浓度关系叙述正确的是( )
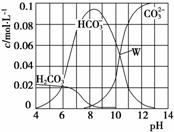
A.W点所示的溶液中:c(CO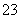 )=c(HCO
)=c(HCO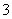 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.pH=4的溶液中:c(H2CO3)+c(HCO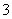 )+c(CO
)+c(CO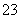 )=0.1 mol·L-1
)=0.1 mol·L-1
C.pH=8的溶液中:c(Na+)>c(HCO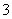 )>c(CO
)>c(CO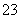 )>c(H2CO3)
)>c(H2CO3)
D.pH=11的溶液中:c(Na+)+c(H+)=c(OH-)+c(Cl-)+c(CO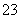 )+c(HCO
)+c(HCO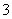 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是
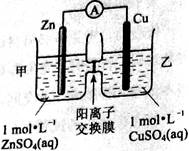
A、 铜电极上发生氧化反应
B、 电池工作一段时间后,甲池的c(SO42-)减小
C、 电池工作一段时间后,乙池溶液的总质量增加
D、 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3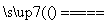 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com