
【题目】实验测得BH3为平面三角形(键角均为120°),NH3为三角锥型(键角为107.3°),已知电子数相同的微粒具有相似的结构。由此推断:①甲基,②甲基碳正离子(![]() ),③甲基碳负离子(
),③甲基碳负离子(![]() )的键角相对大小顺序为( )
)的键角相对大小顺序为( )
A.②>①>③B.①>②>③
C.③>①>②D.①=②=③
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】磷酸亚铁![]() 为白蓝色晶体,溶于强酸,不溶于水和乙醇。它是生产
为白蓝色晶体,溶于强酸,不溶于水和乙醇。它是生产![]() 的原料,实验室利用
的原料,实验室利用![]() 、
、![]() 及
及![]() 为原料制备磷酸亚铁的实验流程如图1:
为原料制备磷酸亚铁的实验流程如图1:
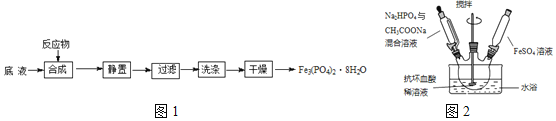
合成时的主要反应为:![]()
![]() 实验中由原料配制溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是______。
实验中由原料配制溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是______。
![]() 合成时,在三口烧瓶中先加入抗坏血酸
合成时,在三口烧瓶中先加入抗坏血酸![]() 稀溶液作底液,再向烧瓶中,滴入
稀溶液作底液,再向烧瓶中,滴入![]() 与
与![]() 混合溶液至
混合溶液至![]() 时,再滴入
时,再滴入![]() 溶液,最终维持
溶液,最终维持![]() 装置如图2所示
装置如图2所示![]() 。
。
![]() 实验不是将三种溶液直接混合的原因是______。
实验不是将三种溶液直接混合的原因是______。
![]() 用抗坏血酸溶液作底液而不用铁粉,其主要原因是______。
用抗坏血酸溶液作底液而不用铁粉,其主要原因是______。
![]() 生成的
生成的![]() 沉淀需充分洗涤,检验洗涤是否完全的方法是______
沉淀需充分洗涤,检验洗涤是否完全的方法是______
![]() 检验产品中是否混有
检验产品中是否混有![]() 或
或![]() 杂质的方法是______。
杂质的方法是______。
![]() 某研究性学习小组的同学拟用工业品十二水合磷酸氢二钠
某研究性学习小组的同学拟用工业品十二水合磷酸氢二钠![]() 含
含![]() 、重金属盐及有色杂质等
、重金属盐及有色杂质等![]() 提纯得到
提纯得到![]() 晶体。已知:
晶体。已知:![]() 溶液pH
溶液pH![]() ,重金属硫化物不溶于水。
,重金属硫化物不溶于水。
请补充实验步骤
![]() 实验中必须使用的试剂有:
实验中必须使用的试剂有:![]() 溶液、活性炭、
溶液、活性炭、![]() 溶液、乙醇
溶液、乙醇![]() 磷酸氢二钠在水中溶解度
磷酸氢二钠在水中溶解度![]() 水
水![]()
温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|
|
|
|
| |||||||
|
| ||||||||||
|
|
|
|
|
| ||||||
|
|
将工业品溶于适量热水,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯原子对O3的分解有催化作用:
O3+Cl=ClO+O2 ΔH1
ClO+O=Cl+O2 ΔH2
该反应的能量变化如图所示,下列叙述中正确的是( )

A.反应O3+O=2O2的ΔH=E1-E2
B.反应O3+O=2O2的ΔH=E2-E3
C.反应O3+O=2O2是吸热反应
D.反应O3+O=2O2的ΔH=ΔH1+ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。

请回答下列问题:
(1)在“图1”中,曲线____填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g)![]() CH3OH(g)的△H= _________________________ 。
CH3OH(g)的△H= _________________________ 。
(2)下列说法正确的是 (_________)
A.起始充入的CO的物质的量为1mol
B.增加CO的浓度,H2的转化率会增大
C.容器中压强恒定时,反应达到平衡状态
(3)从反应开始到建立平衡,υ(CO)= _______;达到平衡时,c(H2)= ____ ,该温度下CO(g)+2H2(g) ![]() CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应的是( )
A.MgCl2 + Ba(OH)2 == BaCl2 + Mg(OH)2↓B.CO2 + 2NaOH == Na2CO3 + H2O
C.CaCO3 ![]() CaO + CO2↑D.H2 + CuO ==H2O + Cu
CaO + CO2↑D.H2 + CuO ==H2O + Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理应用和处理含氮的化合物,在生产、生活中有重要意义。回答下列问题:
(1)在紫外光照射的条件下,氯气与偏二甲肼[(CH3)2NNH2]可快速反应,偏二甲肼转化为CH3OH和N2,该反应的化学方程式为______________________________。
(2)连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。25℃时,连二次硝酸的电离常数Ka1=6.17×10-8,Ka2=2.88×10-12
①25℃时0.1molL-1NaHN2O2溶液中离子浓度由大到小的顺序为____________________________。
②25℃时向0.1 molL-1连二次硝酸溶液中逐滴滴入NaOH溶液,当溶液的pH=10时,C(N2O22-)/ C(H2N2O2)=________。
(3)亚硝酰氯可由NO与Cl2反应制得,反应原理为2NO(g)+ Cl2 (g)![]() 2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
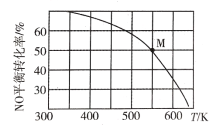

①该反应的△H_____(填“>”“<”或“=”)0。
②M点时容器内NO的体积分数为____。
③若反应一直保持在P压强条件下进行,则M点的平衡常数Kp=____________,(用含P的表达式表示)。
(4)工业上电解NO制备NH4NO3可以变废为宝,其工作原理如图所示、电解时阳极反应式为___________,为使电解产物全部转化为NH4NO3,需要补充物质A,物质A化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有单质A、B、C及化合物D、E、F、G、H,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。
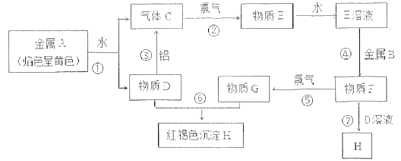
请根据以上信息回答下列问题:
(1)反应③是D物质的水溶液与金属铝反应,金属铝被氧化___(写化学式);
(2)步骤⑦中刚生成的白色沉淀颜色会迅速发生变化,最终生成红褐色沉淀H,请写出由白色沉淀变成H的化学方程式:___;
(3)检验G中所含的金属离子时,在G溶液中加入硫氰化钾溶液,离子方程式为:___;
(4)工业上将氯气通入D溶液中制取消毒液,反应的化学方程式为___,1mol氯气发生反应,转移电子___mol;消毒液中的有效成分是___(填名称);
(5)将0.1molA的碳酸盐溶液和0.15molE溶液混合,有如下两种方式:
A.将含A的碳酸盐溶液逐滴加入到E溶液中;
B.将E溶液逐滴加入到含A的碳酸盐溶液中;
理论上产生气体比较多的是___(填序号),多___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是( )
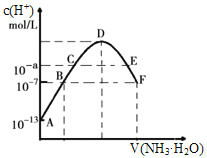
A. NaHB溶液可能为酸性,也可能为碱性
B. A、B、C三点溶液的pH是逐渐减小,D、E、F三点溶液的pH是逐渐增大
C. E溶液中离子浓度大小关系:c(NH4+)>c(B2-)>c(OH-)>c(H+)
D. F点溶液c(NH4+)=2c(B2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚乙酯是一种重要的添加剂,其结构简式为![]() 。用环氧乙烷合成碳酸亚乙酯的反应为:
。用环氧乙烷合成碳酸亚乙酯的反应为: 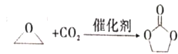 下列说法错误的是
下列说法错误的是
A.碳酸亚乙酯中的所有原子处于同一平面内B.碳酸亚乙酯的二氯代物只有两种
C.上述反应属于加成反应D.1 mol碳酸亚乙酯最多可消耗2 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com