
| A. | 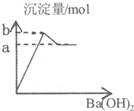 图表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀的量关系曲线 | |
| B. | 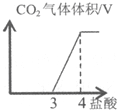 图表示向含有等物质的量的NaOH和Na2CO3溶液中加入盐酸放出CO2的关系曲线 | |
| C. | 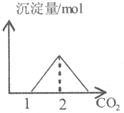 图表示向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2的产生沉淀关系曲线 | |
| D. |  图表示向NaOH溶液中滴加AlCl3溶液产生沉淀的量关系曲线 |
分析 A.向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,反应生成硫酸钡、氢氧化铝、硫酸钾\继续滴加,氢氧化铝溶解;
B.对NaOH和Na2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钠与盐酸的中和反应,再发生碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠,最后发生碳酸氢钠与盐酸反应才有二氧化碳气体生成,利用物质的量的关系并结合图象即可解答;
C.向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2,二氧化碳和氢氧化钙反应生成碳酸钙沉淀,当氢氧化钙消耗完时,继续通入二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠,当氢氧化钠完全反应后,继续通入二氧化碳,二氧化碳和碳酸钠、水反应生成碳酸氢钠,当碳酸钠反应后,继续通入二氧化碳,二氧化碳和和碳酸钙、水反应生成可溶性的碳酸氢钙,根据反应2OH-+CO2═CO32-+H2O,Ca2++CO32-═CaCO3↓,CO32-+CO2+H2O═2HCO3-,CaCO3+CO2+H2O═Ca(HCO3)2判断;
D.向NaOH溶液中滴加AlCl3溶液,氢氧根离子过量,开始无沉淀生成,随反应进行氢氧根离子消耗完,继续滴加氯化铝溶液,铝离子和偏铝酸根离子双水解生成氢氧化铝沉淀.
解答 解:A.向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,离子方程式为:2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓,继续滴加,则发生Al3++4OH-═AlO2-+2H2O,图象变化趋势符合,故A正确;
B.向等物质的量NaOH和Na2CO3混合溶液中滴加盐酸时,首先和NaOH反应生成水和氯化钠,当滴入先发生氢氧化钠与盐酸的中和反应,两者恰好反应后,H++OH-=H2O,继续滴加时,盐酸和Na2CO3开始反应,首先发生HCl+Na2CO3=NaHCO3+NaCl,不放出气体,当再加入时,此步反应进行完全;继续滴加时,发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑;此时开始放出气体,未生成气体消耗HCl和生成气体消耗HCl物质的量之比为2:1,不与图象相符,故B错误;
C.向含有等物质的量的Ca(OH)2、NaOH的混合溶液中通入CO2至沉淀消失,发生的反应分别为2OH-+CO2═CO32-+H2O,Ca2++CO32-═CaCO3↓,CO32-+CO2+H2O═2HCO3-,CaCO3+CO2+H2O═Ca(HCO3)2,设Ca(OH)2的物质的量为xmol,则各段反应消耗的二氧化碳的物质的量分别为x,1.5x,x比值为2:3:2,图象不符合,故C错误;
D.向NaOH溶液中滴加AlCl3溶液,氢氧根离子过量,Al3++4OH-=AlO2-+H2O,开始无沉淀生成,随反应进行氢氧根离子消耗完,继续滴加氯化铝溶液,铝离子和偏铝酸根离子双水解生成氢氧化铝沉淀,Al3++3AlO2-+6H2O=4Al(OH)3↓,图象不符合,故D错误;
故选A.
点评 本题考查物质之间的反应,明确物质的性质、及反应先后顺序,图象中变化的特征和反应定量关系确定是解本题关键,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | CuO作还原剂 | B. | CuO作氧化剂 | ||
| C. | 铜元素被氧化 | D. | 铜元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量CO2通入NaOH溶液中:CO2+2OH-═CO32-+H2O | |
| B. | 铜与足量浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO↑+2H2O | |
| C. | 碳酸钠固体溶于水:CO32-+2H2O?H2CO3+2OH- | |
| D. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制的七个物理量之一 | |
| B. | 摩尔是表示物质质量的单位 | |
| C. | 科学上规定含有阿伏加德罗常数个粒子的任何粒子集合体为1mol | |
| D. | 1mol氧含6.02×1023个O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 按要求完成下列问题:
按要求完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
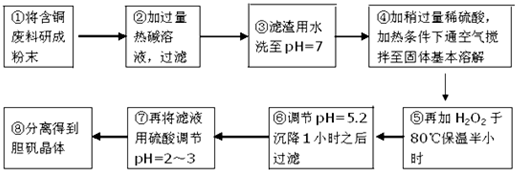
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 | Fe(OH)2 |
| pH | 5.2 | 3.1 | 6.7 | 9.4 | 9.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com