
【题目】锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液的化学方程式:__________________________。
(2)锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为_________(用化学式表示)。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是_______________。
① 硫酸铝和氢氧化钠 ② 硫酸锌和氢氧化钠 ③硫酸铝和氨水 ④ 硫酸锌和氨水
(4)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另一种耐高温的物质,写出该反应的化学方程式:__________。
(5)某混合物![]() ,含有
,含有![]() 、
、![]() 和
和![]() ,在一定条件下可实现如图所示的物质之间的变化:
,在一定条件下可实现如图所示的物质之间的变化:
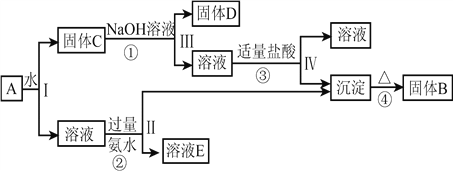
据此回答下列问题:
①写出固体![]() 的化学式:
的化学式: ![]() __________;
__________;
②写出D与稀硫酸反应的化学方程式:___________________________________________;
写出反应①的离子方程式:_________________________________________。
【答案】 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Na2ZnO2 ①②④ 4Al+3C+3TiO2![]() 2Al2O3+3TiC Al2O3 Fe2O3+ 3H2SO4
2Al2O3+3TiC Al2O3 Fe2O3+ 3H2SO4![]() Fe 2(SO4) 3+ 3H2O Al2O3 + 2OH
Fe 2(SO4) 3+ 3H2O Al2O3 + 2OH ![]() 2AlO2+ H2O
2AlO2+ H2O
【解析】(1)单质铝与氢氧化钠溶液反应生成偏氯酸钠和氢气,反应的方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。(2)迁移铝与氢氧化钠溶液的反应写出锌和氢氧化钠溶液反应的化学方程式为Zn + 2NaOH=Na2ZnO2+H2↑,所以锌和氢氧化钠溶液反应后,溶液中锌元素的存在形式为Na2ZnO2。(3)① 将硫酸铝溶液逐滴加入氢氧化钠溶液至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氢氧化钠溶液逐滴加入硫酸铝溶液中先生成白色沉淀,氢氧化钠过量后氢氧化铝后消失。可以鉴别。②将硫酸锌溶液逐滴加入氢氧化钠溶液至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氢氧化钠溶液逐滴加入硫酸锌溶液中先生成白色沉淀,氢氧化钠过量后氢氧化锌后消失。可以鉴别。③硫酸铝和氨水,无论滴加顺序如何,均生成氢氧化铝白色沉淀,无法鉴别。④将硫酸锌溶液逐滴加入氨水中至过量,一开始不产生沉淀,最终生成氢氧化铝沉淀;将氨水逐滴加入硫酸锌溶液中先生成白色沉淀氢氧化锌后消失。可以鉴别。选①②④。(4)根据信息知铝粉与石墨、TiO2在高温下反应生成TiC和Al2O3,该反应的化学方程式为4Al+3C+3TiO2![]() 2Al2O3+3TiC。(5)将混合物A溶于水,过滤,溶液为硫酸铝钾溶液,固体C为氧化铁和氧化铝的混合物,加入氢氧化钠溶液,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,固体D为氧化铁,向偏铝酸钠溶液中加入适量盐酸,二者发生反应生成氢氧化铝沉淀和氯化钠,氢氧化铝受热分解生成氧化铝和水,固体B为氧化铝;向硫酸铝钾溶液加入过量氨水,生成氢氧化铝沉淀和硫酸钾、硫酸铝的混合液,则①固体B为Al2O3;②D为氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水,化学方程式为Fe2O3+ 3H2SO4=Fe 2(SO4) 3+ 3H2O;氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3 + 2OH =2AlO2+ H2O。
2Al2O3+3TiC。(5)将混合物A溶于水,过滤,溶液为硫酸铝钾溶液,固体C为氧化铁和氧化铝的混合物,加入氢氧化钠溶液,氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,固体D为氧化铁,向偏铝酸钠溶液中加入适量盐酸,二者发生反应生成氢氧化铝沉淀和氯化钠,氢氧化铝受热分解生成氧化铝和水,固体B为氧化铝;向硫酸铝钾溶液加入过量氨水,生成氢氧化铝沉淀和硫酸钾、硫酸铝的混合液,则①固体B为Al2O3;②D为氧化铁,氧化铁与稀硫酸反应生成硫酸铁和水,化学方程式为Fe2O3+ 3H2SO4=Fe 2(SO4) 3+ 3H2O;氧化铝和氢氧化钠溶液反应生成偏铝酸钠和水,离子方程式为Al2O3 + 2OH =2AlO2+ H2O。


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是宝贵的自然资源,水的净化与污水处理是化学工作者需要研究的重要课题。
(1)在净水过程中用到混凝剂,其中不可以作为混凝剂使用的是__________。
A.硫酸铝 B.氧化铝 C.碱式氯化铝 D.氯化铁
(2)海水淡化是人类获得饮用水的一个重要方法,下列有关海水淡化处理的方法正确的是_____。
A.蒸馏法能耗最小,设备最简单;冷冻法要消耗大量能源
B.利用电渗析法淡化海水时,在阴极附近放阴离子交换膜,在阳极附近放阳离子交换膜
C.利用电渗析法淡化海水时,得到淡水的部分在中间区
D.利用反渗透技术可以大量、快速地生产淡水
(3)除了水资源,能源、信息、材料一起构成了现代文明的三大支柱。甲醇是一种重要的化工原料,以甲醇、氧气为基本反应物的新型燃料电池已经问世,其结构如图所示(甲醇解离产生的H+可以通过质子交换膜进入另一极)。请写出通入甲醇的电极上的电极反应式:____________。

某同学以甲醇燃料电池为电源,以石墨为电极电解500mL 0.2mol·L1 CuSO4溶液,则与电源正极相连的电解池电极上的电极反应式为:_______________________________;电解一段时间后,在电解池两极上共产生7.84 L气体(标准状况下),此时甲醇燃料电池中共消耗甲醇_________g 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中含有Mg2+、Ba2+ 、Ag+和NO3-,现分别用NaCl溶液、NaOH溶液和Na2CO3溶液将溶液中三种阳离子逐一完全沉淀分离,其流程如右图所示。下列说法正确的是( )

A. 试剂A可能为NaOH溶液
B. 沉淀2只能是BaCO3 ,不可能是Mg(OH)2
C. 每加一种试剂需过量但不需要过滤即可进行下一步
D. 生成沉淀1的离子方程式只能是:Ag+ + Cl- = AgCl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源紧张、资源短缺、环境恶化是当今世界面临的三大问题,下列说法错误的是
A.电池外壳的金属材料回收再利用
B.将地沟油回收再加工为食用油,提高资源的利用率
C.目前我国使用的主要能源是化石燃料,化石燃料属于不可再生能源
D.能源的开发和利用情况,可以衡量一个国家或地区的经济发展和科学技术水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是烃,有机物B易溶于水,且1 mol B能跟足量的钠反应生成标准状况下的H2 11.2 L,但不能与NaHCO3溶液反应,已知A通过如下转化关系可制得化学式为C4H8O2的酯E,且当D―→E时,相对分子质量增加28。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
请回答下列问题:
(1)反应①的原子利用率为________。
(2)B的密度比水________,B中含氧官能团的名称为________。
(3)反应②的化学方程式为________________________________。
(4)反应③的反应类型为______________________。
(5)4.4 g C物质完全燃烧消耗________ mol氧气。
(6)若D―→E时,式量增加m,则B的相对分子质量为__________ (用含m的代数式表示) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述正确的是
A. 0.5mol雄黄(As4S4,已知As和N同主族,结构如右图)含有NA个S—S键
B. 46g乙醇溶液中,所含的氧原子数为NA
C. 1mol二氧化碳分子中共用电子对数为4NA
D. 标准状况下,含NA个氩原子的氩气的体积约为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池以熔融金属Na、熔融S和多硫化钠[Na2Sx(3<x<5)]分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质。下列关于该电池的叙述错误的是( )
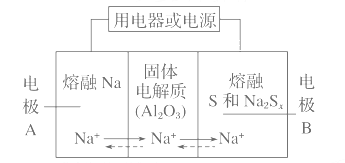
A. 放电时,电极B为正极
B. 充电时内电路中Na+的移动方向为从B到A
C. 该电池的工作适宜温度应该在Al2O3的熔点和沸点之间
D. 充电时阳极反应为S![]() -2e-===xS
-2e-===xS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于能源,以下说法中不正确的是
A.煤、石油、天然气等燃料属不可再生能源
B.煤、石油、水煤气可从自然界直接获取,属一级能源
C.太阳能是一级能源、新能源、可再生能源
D.潮汐能来源于月球引力做功
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com