
某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成了如下实验:

另取10.80 g X在惰性气流中加热至完全分解,得到6.40 g固体1。
请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图________,写出气体甲的电子式________。
(2)X的化学式是________,在惰性气流中加热X至完全分解的化学反应方程式为____________________。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是____________________(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式____________________,并设计实验方案验证该反应的产物____________________。
解析:因X与盐酸反应生成气体甲,则X应为弱酸盐,又因X受热分解可生成气体甲和固体1,可推知固体1应为金属氧化物。因固体1中有与水反应的物质,且溶液1中通入气体甲先出现白色沉淀1后溶解,可推知固体1中含有CaO,气体甲为CO2。根据白色沉淀2遇到空气变为红褐色沉淀,可知X中含有Fe2+。综上分析,X应含有FeCO3和CaCO3。
(1)白色沉淀1为CaCO3,钙原子的结构示意图为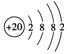 ;CO2为共价化合物,C、O原子间以共价键结合,其电子式为:
;CO2为共价化合物,C、O原子间以共价键结合,其电子式为: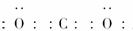 。
。
(2)10.80 g X完全分解生成CO2的质量为10.80 g-6.40 g=4.40 g,其物质的量为0.10 mol,根据CaCO3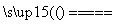 CaO+CO2↑、FeCO3
CaO+CO2↑、FeCO3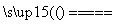 FeO+CO2可得:n(FeO)+n(CaO)=0.1 mol,56 g·mol-1×n(CaO)+72 g·mol-1×n(FeO)=6.40 g,解以上两式可得:n(FeO)=n(CaO)=0.050 mol,则X的化学式为CaFe(CO3)2。X在惰性气流中受热至完全分解的化学方程式为
FeO+CO2可得:n(FeO)+n(CaO)=0.1 mol,56 g·mol-1×n(CaO)+72 g·mol-1×n(FeO)=6.40 g,解以上两式可得:n(FeO)=n(CaO)=0.050 mol,则X的化学式为CaFe(CO3)2。X在惰性气流中受热至完全分解的化学方程式为
CaFe(CO3)2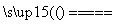 CaO+FeO+2CO2↑。
CaO+FeO+2CO2↑。
(3)Fe(OH)2被空气中的O2氧化为Fe(OH)3,其化学方程式为4Fe(OH)2+O2+2H2O===4Fe(OH)3。
(4)CO2具有氧化性,而FeO具有还原性,两者可发生氧化还原反应,可能的化学方程式为CO2+2FeO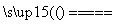 Fe2O3+CO。
Fe2O3+CO。
根据Fe3+与KSCN溶液的特征反应检验产物中的Fe2O3;利用CO的还原性检验产物中的CO。
答案:(1)
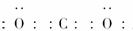
(2)CaFe(CO3)2 CaFe(CO3)2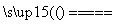 CaO+FeO+2CO2↑
CaO+FeO+2CO2↑
(3)4Fe(OH)2+2H2O+O2===4Fe(OH)3
(4)2FeO+CO2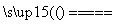 Fe2O3+CO
Fe2O3+CO
检测Fe2O3:将固体用稀盐酸溶解,加入KSCN溶液若显红色,表明产物中有Fe(Ⅲ)
检测CO:将气体通过灼热CuO,黑色固体变为红色
点拨:知识:元素化合物的性质[CaCO3、FeCO3的分解反应,Fe(OH)2与O2的反应,Ca(OH)2与CO2的反应]、氧化还原反应、原子结构示意图和电子式。能力:综合应用所学元素化合物知识推断物质的能力;书写原子结构示意图、电子式和化学方程式的能力;设计简单实验方案的能力。试题难度:中等。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度
C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度。假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小
D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是一种综合处理SO2废气的工艺流程。下列说法正确的是( )
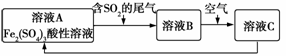
A.向B溶液中滴加KSCN溶液,溶液变为血红色
B.溶液B转化为溶液C发生的变化的离子方程式为4H++4Fe2++O2===4Fe3++2H2O
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
科目:高中化学 来源: 题型:
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
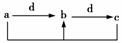
| 物质 选项 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | CH3CH2OH | CH3CHO | CH3COOH | O2 |
| C | Na2CO3 | NaHCO3 | NaOH | CO2 |
| D | Cl2 | FeCl3 | FeCl2 | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应离子方程式正确的是( )
|
| A. | 过量石灰水与碳酸氢钙反应:Ca2++2HCO3﹣+2OH﹣═CaCO3↓+CO32﹣+2H2O |
|
| B. | FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O |
|
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═AlO42﹣+4NH4++2H2O |
|
| D. | H2SO4与Ba(OH)2溶液反应:Ba2++OH﹣+H++SO42﹣═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是( )

|
| A. | 向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液中加入0.1 mol/L稀H2SO4溶液 |
|
| B. | 向含有0.1 mol/L AlCl3和0.3mol/L NH4Cl的1L混合液中加入0.1mol/L NaOH溶液 |
|
| C. | 向烧碱溶液中滴加明矾溶液 |
|
| D. | 向Ca(OH)2溶液中逐渐通入二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时,将6 mol CO2和8 mol H2充入2 L密闭容器中,发生反应CO2(g)+H2(g)  CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
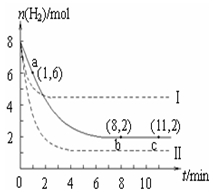
A.反应开始至a点时v(H2)=1 mol·L-1·min-1
B.若曲线Ⅰ对应的条件改变是升温,则该反应DH>0
C.曲线Ⅱ对应的条件改变是降低压强
D.T ℃时,该反应的化学平衡常数为0.125
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com