
| A. | 食盐、食醋和味精是常用的食品添加剂,其主要成分均属钠盐 | |
| B. | SO2、CO2、NO2均被列入我国空气质量报告的指标 | |
| C. | 提倡人们购物时不用塑料袋,是为了防止白色污染 | |
| D. | 家用84消毒液可用来漂白衣物,为了增强其漂白效果,使用时可加入浓盐酸 |
分析 A.食醋主要成分为乙酸;
B.二氧化碳能导致温室效应,但二氧化碳无毒,不属于空气污染物;
C.白色污染是指废旧塑料制品带来的污染,提倡人们购物时不用塑料袋;
D.家用84消毒液能与浓盐酸反应产生氯气.
解答 解:A.食盐、食醋和味精是常用的食品添加剂,食盐和味精(谷氨酸的钠盐)其主要成分均属钠盐,食醋主要成分为乙酸,不是钠盐,故A错误;
B.二氧化碳能导致温室效应,但二氧化碳无毒,不属于空气污染物,则没有列入我国空气质量报告,而二氧化硫、可吸入颗粒物、二氧化氮都列入我国空气质量报告中,故B错误;
C.白色污染是指废旧塑料制品带来的污染,提倡人们购物时不用塑料袋,能防止白色污染的产生,故C正确;
D.家用84消毒液能与浓盐酸反应产生氯气,为了增强其漂白效果,不可加浓盐酸,故D错误;
故选C.
点评 本题考查物质的组成、性质与用途,把握常见物质的性质与用途等为解答的关键,选项D为易错点,题目难度不大.


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题

| A. | 甲、乙、丙、丁 | B. | 丙、丁、乙、甲 | C. | 丙、丁、甲、乙 | D. | 丁、丙、乙、甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X>Z>Y | B. | Z>Y>X | C. | X>Y>Z | D. | Z>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.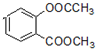 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+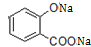 +H2O.
+H2O.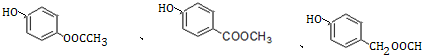 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过滤的方法分离溶液和胶体 | |
| B. | 用四氯化碳萃取碘水中的碘 | |
| C. | 用蒸馏的方法将自来水制成蒸馏水 | |
| D. | 用加热的方法分离氯化钠和单质碘固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应为化合反应 | |
| B. | “通路”是胶体对光产生的丁达尔现象 | |
| C. | 上述反应为氧化还原反应 | |
| D. | 产生的臭氧有毒,会严重影响人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中共消耗1.75 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为1:4 | ||
| C. | 反应中共消耗65 g Zn | D. | 反应中共转移3.6 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+28.7 kJ/mol | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-28.7 kJ/mol | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.4 kJ/mol | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
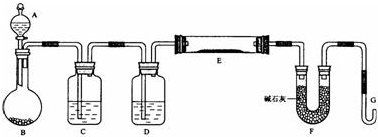
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com